새로운 치료 타겟 제공으로 신개념 간암 치료제 개발 기대
국내 연구진이 사망률과 발생 빈도가 높은(5대 암 중 사망률 2위, 발생빈도 5위) 간암의 억제 유전자* 기능을 규명하여 간암 치료제 개발에 획기적인 전환점을 마련하였다. 특히 이번 연구는 간암 치료제가 거의 없는 상황에서 다양한 요인으로 발생하는 간암 환자에게 활용할 수 있다는 점에서 그 의의가 매우 크다.
* 암 억제 유전자: 정상세포에 존재하며 그 세포가 암세포화되는 것을 막는 유전자.
암 억제 유전자들이 돌연변이 또는 여러 다른 원인에 의해 기능을 잃게 되면 암이 발병하게 된다.

가톨릭의대 남석우 교수와 배현진․정광화 박사(공동 제1저자)가 참여한 이번 연구는 미래창조과학부(장관: 최양희) 포스트게놈 다부처 유전체 사업의 지원을 통해 수행되었고, 의약학 분야 권위지인 간장학(肝臟學) 저널(Journal of Hepatology, IF: 10.401) 온라인 판(3월 28일)에 게재되었다.
국내․외에서 간암은 다섯 번째로 많이 발생하는 암(발생률 7.6%)으로 흔하게 발생하는 다른 암(갑상선암, 대장암, 위암 등)에 비해 치료 후 생존률*(5년 후, 28.6%)이 현저히 낮고 자각증상이 없어 조기진단이 어려운 악성 암종이다
* 5년 생존율 : 암 환자가 특정 암 치료를 받은 날부터 '5년 후에도 생존할 확률(갑상선암 100%, 대장암 73.8%, 위암 69.4%, 폐암 15.4%)
현재까지 알려진 가장 효과적인 치료법은 간 절제술이나 간암 초기에만 가능하다는 단점이 있고 공인된 약물 치료제*는 단 한가지로 다양한 원인에 의해 발생하는 모든 간암 환자들에게 적용하기에는 한계가 있다고 한다.
* sorafenib: 미국식품의약국(FDA) 승인 완화치료제로 현재 사용되고 있는 항암제
연구팀은 암 억제 유전자 히스톤 탈아세틸화 효소 6(HDAC6*: Histone deacetylase 6)이 마이크로리보핵산-221(microRNA**-221, miR-221)의 억제나 발현에 따라 간 암세포의 성장(억제나 성장)이 유도된다는 사실을 규명하였다.
* HDAC6(Histone deacetylase 6, 히스톤 탈아세틸화효소 6) : 아세틸기(CH3CO–)를 가지고 있는 단백질에서 아세틸기를 떼어내는 효소 중 하나
* microRNA : 단백질로 전사되지 않는 17~25 염기서열로 구성된 작은 RNA 조각으로 miR-221은 221번째로 발견된 microRNA를 의미함
마이크로리보핵산-221(microRNA-221, miR-221)을 선택적으로 억제하였을 때 스톤 탈아세틸화 효소 6(HDAC6: Histone deacetylase 6)의 발현이 증가하여 암세포의 성장이 억제되었고, 마이크로리보핵산-221(microRNA-221, miR-221)의 발현을 높였을 때 스톤 탈아세틸화 효소 6(HDAC6: Histone deacetylase 6)의 발현이 감소되어 암세포가 성장된다는 것을 발견하였다.
향후, 암 억제 유전자의 활성화를 방해하는 마이크로리보핵산-221(microRNA-221, miR-221)의 발현 기전을 인체 부작용 없이 조절하여 간암 세포를 제거하는 치료제의 개발이 가능할 것으로 기대된다.
간암발생에 있어 매우 강력한 암 억제 유전자인 톤 탈아세틸화 효소 6(HDAC6: Histone deacetylase 6)의 기능소실 원리를 규명함으로써
간세포 내 암 억제 유전자의 기능을 방해하는 과정을 제어하는 새로운 개념의 간암치료 방법을 제시했다는 점에서 의의가 크며,
간암 발생이나 간암세포의 성장을 막을 수 있는 치료제 개발에 큰 전환점이 마련되어 창조경제 핵심성과 창출이 기대된다.
연 구 결 과 개 요
1. 연구배경
간암은 한국인에게 발생하는 대표적인 암 중의 하나로서 높은 사망률과 발병률을 보이며, 특히 진행성 간암인 경우 매우 낮은 5년 생존률 (5-year survival rate)로 예후가 극히 불량한 암종의 하나이다. 간암은 국내 암 질환 중 사망률에서는 폐암에 이어 2위를 차지하고 있고(15.4%), 우리나라에서 발병하는 암 중 발생 빈도로 5위를 차지하고 있으며 우리나라 40, 50대 남성 사망률 1위를 차지하고 있다. 간암은 발생 초기 자각증상이 없어 조기 진단이 어렵고, 치료방법이 매우 제한되어있다. 또한 현재까지 공인된 간암 치료제는 단 한 가지로서, 다양한 원인에 의해 발생하는 간암 환자들에 모두 적용하기에는 그 한계가 분명하다. 따라서, 본 연구에서는 간암 치료에 표적 기전으로 사용할 수 있는 새로운 분자적 기전을 제시하고자 하였다.
2. 연구내용
본 연구팀은 정상 조직과 비교하여 간암 조직에서 발현이 증가되어 있는 microRNA인 miR-221이 HDAC6의 발현 소실을 유도한다는 사실을 확인하였다(그림 1 참조). 그리고, 간암세포주에서 miR-221을 선택적으로 억제하였을 때, HDAC6에 의해 유도되는 자가포식 작용에 의해 암세포의 성장이 억제된다는 사실을 확인하였다(그림2 참조).
또한 c-Met/JNK/c-Jun 신호전달경로와, NF-κBp65 전사인자에 의하여, 간암에서 miR-221이 과발현되고, 그에 따라 HDAC6의 발현이 저해됨을 확인하였으며, 최종적으로 약물 유래 간암 랫드 모델과, 형질전환 간암 마우스 모델, 그리고 인체 시료에서 모두 c-Met/JNK/c-Jun 및 NF-κBp65 에 의하여 miR-221의 발현 증가와 HDAC6의 발현 소실이 이루어짐을 확인하였다(그림 3참조).
3. 기대효과
본 연구를 통해 간암 억제 유전자인 HDAC6의 소실을 유도하는 기전이 존재한다는 것을 밝혀내었고, 이를 동물 모델 및 인체 시료에서 검증하였다. 이는 HDAC6의 통합적 발현 조절 기전을 규명함으로써 신개념의 유전자 발현 조절 기전을 제시하였다는 것에 그 의의가 있으며, 새로운 간암 치료제가 개발될 수 있는 표적 기전을 제공하여, 간암 치료에 획기적인 전환점을 제시해 줄 수 있으리라 생각된다.
연 구 결 과 문 답
이번 성과 뭐가 다른가
간암 특이 암 억제 유전자인 HDAC6가 소실되는 기전을 규명하였고, 이를 동물모델에서 검증하였다. 간암 치료에 특이적으로 이용할 수 있다는 측면에서 그 의미가 크다.
어디에 쓸 수 있나
먼저 간암 발생이나 간암 세포의 성장을 막을 수 있는 간암 치료제 개발의 새로운 표적 기전으로 사용될 수 있다. 현재 간암 치료제가 현저히 부족한 상황에서, 획기적인 표적 기전으로 작용할 수 있다.
실용화를 위한 과제는
c-Met/JNK/c-Jun 신호전달 체계 및 NF-κB 억제 시 일어날 수 있는 부작용을 줄이기 위하여, 해당 신호전달 체계가 활성화되어 있는 세포에 대하여 정확하게 작용할 수 있는 치료제 개발이 필요하다.
연구를 시작한 계기는
기존에 제시된 간암 치료제들이 가진 문제점을 보완하기 위해서는 새로운 표적 기전의 발굴이 필요하다. 특히 HDAC6는 다른 암종에서와 달리 간암 특이적으로 암 억제 유전자로 작용할 수 있으므로, HDAC6의 발현을 회복시킨다면 간암 치료에 대한 효과적인 표적 기전이 될 수 있을 것이라 생각하였다. 특히 간암 조직에서 miR-221의 발현이 증가되어 있다는 사실을 토대로 이 물질에 의하여 HDAC6의 기능이 억제되고 있을 것이라는 점에 착안하였다.
꼭 이루고 싶은 목표는
기존 연구와 본 연구를 토대로 하여, 분자적인 수준에서의 간암의 발생 및 진행 기전을 밝히는 것이 첫 번째 목표이고, 이를 토대로 간암에서 효과적인 치료를 유도할 수 있는 새로운 표적 기전을 제시하는 것이 최종 목표이다.
용 어 설 명
1. Journal of Hepatology 지
Elsevier 사가 매월 발간하는 저명한 간 학술지(Impact factor: 10.401).
2. 마이크로 RNA(microRNA)
17~25개의 염기로 구성되는, 단백질로 번역되지 않는 단일가닥 RNA 절편
3. HDAC6(Histone deacetylase 6, HDAC6)
히스톤 탈아세틸화효소(Histone deacetylases) 단백질군에 속하는 효소로써, 세포 내 미세소관을 구성하는 α- 튜불린(tubulin)을 기질로 반응하며, 암세포의 이동 및 침윤 현상을 조절하여 암세포의 전이에 연관되는 것으로 알려져 있다. 대부분의 암에서 암 유발 유전자로 기능하나, 간암에서는 암 억제 유전자로서 기능한다는 사실을 밝힌 바 있다.
4. c-Met/JNK/c-Jun pathway
간세포 성장인자(Hepatocyte growth factor, HGF)에 의해 활성화되는 세포 내 신호전달체계이다. HGF의 발현이 증가되어 세포 밖으로 분비되면, HGF의 수용체인 c-Met이 이를 받아들여 활성화되고, 이에 따라 하위 분자들인 JNK, c-Jun이 활성화되어, 전사인자인 c-Jun에 의해 여러 가지 유전자들의 발현이 조절되며, 간암에서는 이 신호전달체계가 비정상적으로 활성화되어 있음이 알려져 있다.
5. NF-κB (Nuclear Factor kappa-B)
유전자 전사를 일으키는 전사인자(transcription factor)중 하나로써, 여러 가지 질병과 관련되어 있는 다양한 유전자들의 전사에 관여한다. 간암을 포함한 여러 암에서 NF-κB의 전사 활성이 증가되어 있음이 보고되어 있으며, 이로 인해 여러 암 유발 유전자들의 발현이 증가되는 것이 알려져 있다.
그 림 설 명
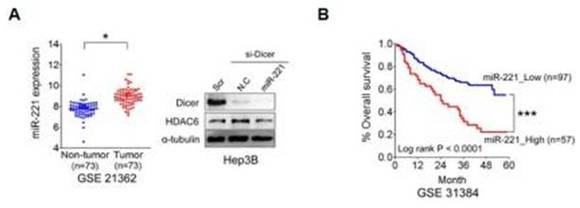
그림 1. 간암에서 miR-221의 발현 증가와 miR-221에 의한 HDAC6 조절
(A) 간암 조직에서 miR-221의 발현이 증가되어 있고 (왼쪽), 간암 세포주에서 miR-221을 인위적으로 증가시켰을 때 HDAC6 단백질 양이 줄어들었다 (오른쪽). (B) miR-221이 과발현되어 있는 대단위 환자군에서의 5년 생존률이 현저히 감소되었다. 이는 간암에서 암 유발 miRNA로 작용하는 miR-221의 과발현에 의하여 HDAC6가 조절되고 있음을 의미함.
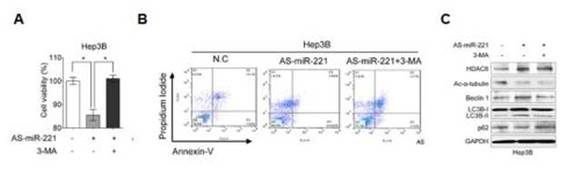
그림 2. miR-221의 억제에 따른 HDAC6 유도 자가포식 기전
(A) 간암 세포주에서 miR-221을 억제하였을 때 세포 성장이 둔해졌고, 여기에 자가포식작용을 막는 3-MA라는 약물을 투여하였을 때 세포 성장이 회복되었다. (B) 동일한 실험군에서의 자가포식작용이 증가되어 세포 성장이 둔해지는 것을 확인하였고, 3-MA투여 후에 자가포식작용이 다시 회복되는 것을 세포 분석을 이용하여 확인하였다. (C) 동일한 실험군에서의 자가포식작용과 연관된 단백질들의 발현 변화를 확인하였다. 이 결과는 간암 세포 내에서 miR-221의 발현이 억제되었을 때, HDAC6 유도 자가포식 기전에 의하여 암세포의 성장이 방해됨을 확인하였으며, 이는 miR-221이 HDAC6 특이적으로 발현을 억제하고 있음을 의미한다.
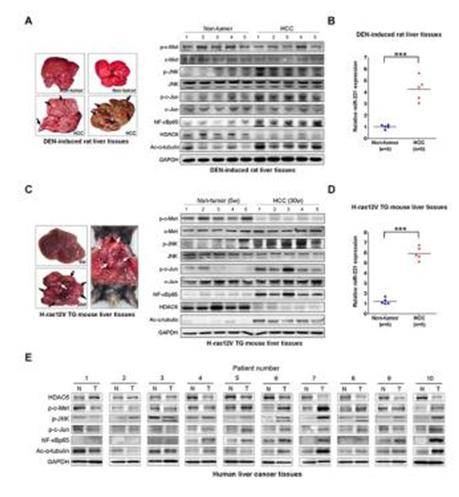
그림 3. 동물 모델 및 간암 환자 조직에서의 miR-221 조절 신호전달 체계에 의한 HDAC6의 발현 억제 확인
(A) Diethylnitrosamine (DEN) 투여 랫드 간암모델을 이용하여 종양 조직에서 정상 조직과 비교하여 c-Met/JNK/c-Jun 및 NF-κB활성 증가 및 HDAC6의 발현 감소를 확인하였다. (B) Diethylnitrosamine (DEN) 투여 랫드 간암모델에서의 miR-221발현이 종양 조직에서 증가됨을 확인함 (C) Ras 형질전환 간암 마우스 모델을 이용하여 종양 조직에서 정상 조직과 비교하여 c-Met/JNK/c-Jun 및 NF-κB활성 증가 및 HDAC6의 발현 감소를 확인함 (D) Ras 형질전환 간암 마우스 모델에서 miR-221의 발현이 종양 조직에서 증가됨을 확인함. (E) 간암 환자의 종양 조직에서 정상 조직과 비교하여 c-Met/JNK/c-Jun 및 NF-κB활성 증가 및 HDAC6의 발현 감소를 확인함. 이는 생체 내에서 c-Met/JNK/c-Jun 신호전달체계 및 NF-κB의 발현 증가에 의하여 miR-221이 증가하고, 이에 따라 HDAC6의 발현이 감소되어 간암 발생 및 진행이 이루어짐을 의미함.
