세포 내 특정 RNA의 리보솜 결합·분리를 제어하는
RNA 광유전학 기술 개발
"Optogenetic control of mRNA localization and translation in live cells "
빛으로 세포 내 특정 RNA 이동과 단백질 합성을 조절할 수 있는 기술이 개발됐다.
기초과학연구원(IBS, 원장 노도영) 인지 및 사회성 연구단(단장 신희섭, 이창준) 허원도 초빙연구위원(KAIST 생명과학과 교수), 이상규 연구위원 연구팀은 빛을 이용해 유전정보를 전달하는 전령RNA와 단백질을 생성하는 리보솜의 결합을 제어하여, 단백질 합성을 조절하는데 성공했다.
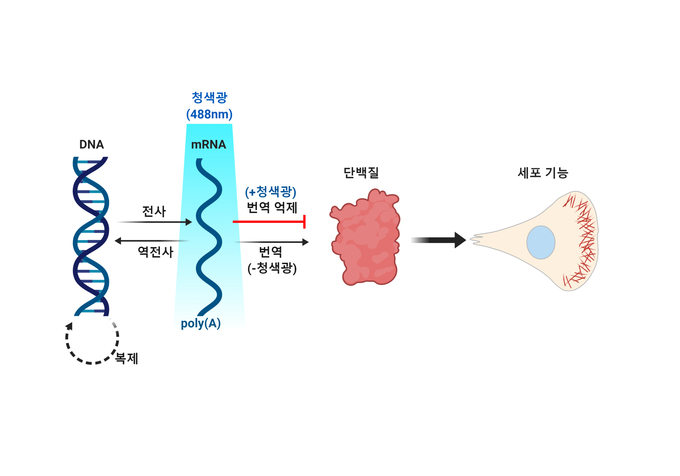
DNA의 유전정보는 RNA1)를 거쳐 단백질로 전달된다. 이 때 중간에서 유전정보를 전달하는 RNA를 ‘전령RNA’라고 한다. 단백질 생성공장인 리보솜은 전령RNA의 유전정보를 읽어 단백질을 합성한다. 단백질 합성에 있어 전령RNA는 DNA 유전정보의 중간 전달자, 리보솜은 생성공장, 단백질은 완성품인 셈이다.
이전에는 화학물질을 처리해 전령RNA를 조절하는 방법으로 모든 전령RNA를 한꺼번에 조절하기 때문에 특정 종류의 전령RNA만을 세밀하게 조절하기 어려웠다. 이번 연구에서는 살아있는 세포에 청색광을 비춰줌으로써 세포 내 특정 전령RNA 이동 및 단백질 합성을 시공간 특이적으로 조절하는 mRNA-LARIAT 광유전학 기술을 개발했다.
연구팀은 이전 연구2)로 개발한 라리아트 올가미(LARIAT, Light-Activated Reversible Inhibition by Assembled Trap) 기술3)을 융합하여 mRNA-LARIAT 기술4)을 개발했다.
mRNA-LARIAT 광유전학 기술을 이용하면 빛의 유무에 따라 라리아트 올가미에 전령RNA를 가두거나 분리하고, 이를 실시간으로 관찰하는 것이 가능하다.
연구팀은 헬라 세포5)에 청색광을 비춰주면 라리아트 올가미에 전령RNA가 가둬지면서 리보솜과 격리되고 단백질 합성이 감소함을 관찰했다. 이어 청색광을 차단하면 라리아트 올가미로부터 전령RNA가 빠져나오면서 리보솜과 단백질 합성을 다시 시작함을 확인했다.
이는 mRNA-LARIAT 광유전학 기술로 빛의 유무에 따라 매우 빠르고 가역적으로 단백질 합성을 조절할 수 있음을 의미한다.
대부분의 단백질은 전령RNA와 리보솜에 의해 합성된 후, 각 단백질이 작용하는 위치로 이동한다. 하지만 전령RNA가 라리아트 올가미에 가둬지면 전령RNA가 향후 단백질이 작용하는 위치까지 이동하는 것이 멈춰지고, 단백질 합성이 차단된다. 이와 같이 mRNA-LARIAT 광유전학 기술을 이용해 빛으로 전령RNA 이동 및 단백질 합성을 조절하면, 살아있는 세포 내 RNA의 위치와 합성되는 신생단백질의 기능을 보다 효율적으로 연구할 수 있다.
연구팀은 베타액틴(β-actin)6) 합성에 관여하는 전령RNA에 mRNA-LARIAT 기술을 적용했다. 베타액틴 단백질 합성에 관여하는 전령RNA에 청색광을 비추니 세포 골격 구성 및 이동 기능이 제대로 이뤄지지 않음을 관찰했다. 또한 베타액틴 단백질 합성 효율이 최대 90%까지 감소됨을 확인했다.
허원도 교수는 “mRNA-LARIAT 광유전학 기술을 활용하면 암세포, 신경세포 등 다양한 세포 내 전령RNA 이동 및 단백질 합성을 빛으로 조절할 수 있다”며 “앞으로 암세포 전이, 신경질환 등 전령 RNA관련 질병 연구에 응용 가능할 것이다”고 말했다.
이번 연구성과는 네이처 셀 바이올로지(Nature Cell Biology, IF 17.728)에 2월 18일 오전 1시(한국시간)자 온라인 판에 실렸으며, Nature Reviews Genetics에 하이라이트 논문으로 소개되었다.
[참고]
1) RNA(Ribonucleic acid) : 모든 생명체에 필수적인 생체고분자물질로, 생명 유지에 필요한 모든 유전정보를 포함하고 있다. 유전자 본체인 DNA로부터 만들어지기 때문에 DNA 유전정보의 복사본이라고 할 수 있다.
2) Reversible protein inactivation by optogenetic trapping in cells. Lee et al. Nat Methods. 2014 Jun;11(6):633-6.
3) 라리아트 올가미(LARIAT, Light-Activated Reversible Inhibition by Assembled Trap) 기술 : 세포에 청색광을 비추면 단백질들이 복합체를 형성해 라리아트 올가미(LARIAT)를 만들어 특정 분자를 가두는 기술
4) RNA 이미징 기술:전령RNA에 형광단백질을 표지하고 현미경으로 관찰함으로써 세포 내 전령RNA 이동을 시각화하는 기술
5) 헬라 세포(HeLa cell) : 사람의 자궁경부암 조직에서 얻어낸 세포계(cell line). HeLa는 환자 이름의 약칭이다. 현존하는 인체에서 유래한 조직배양주 중 가장 오래 전에 분리한 것으로 세계 각지의 연구실에서 배양되며 유지되고 있다. 바이러스학, 암연구, 분자생물학 등의 연구재료로 널리 사용되고 있다.
6) 베타액틴(β-actin) 단백질 : 세포 모양 및 이동에 관여하는 대표적인 세포골격 단백질. 세포 이동 시 세포의 앞부분이나 뒷부분에서 길게 연결되거나 짧게 끊어지면서 세포의 모양을 변화시켜서 세포를 이동하게 함.
연구 추가 설명
논문명/저널명
Optogenetic control of mRNA localization and translation in live cells
Nature Cell Biology
저자정보
Na Yeon Kim, Sankyu Lee, Jeonghye Yu, Nury Kim, Seong Su Won, Hyerim Park and Won Do Heo
연구내용
보충설명
■ 단일 전령RNA 분자의 시공간 특이적 조절을 시각화 하려는 노력에도 불구하고, 특정 전령RNA의 이동 및 단백질 합성을 정확하게 제어하는 데는 어려움이 있었다.
■ 본 연구는 특정 전령RNA 분자를 단백질 복합체(라리아트 올가미)에 포획함으로써 전령RNA의 위치 및 단백질 합성 효율을 조절할 수 있는 RNA 광유전학 기술을 개발했다.
연구 이야기
[연구 배경]
기존에는 화학물질이나 올리고 뉴클레오티드를 처리하여 전령RNA를 조절하였다. 기존의 전령RNA 조절 방법은 세포 내 모든 RNA를 일괄적으로 조절하는 방법으로, 특정 RNA를 조절하기에는 많은 한계점이 있었다. 세포의 이동을 관찰할 때 전령RNA가 어떤 공간에 어떻게 분포하는지를 확인하기 어려웠다. 또한 화학물질 처리의 경우 세척 및 재처리를 하는 과정이 필요했고, 올리고 뉴클레오티드 처리의 경우 그 효과를 나타내기까지 긴 시간이 걸렸다.
이런 한계점을 극복하고, 특정 전령RNA를 시공간 특이적으로 조절하기 위해 RNA 광유전학 기술을 개발하게 되었다.
[어려웠던 점]
특정 전령RNA를 조절하는 기술을 개발했지만, 기술의 효율성을 높이고 효용성을 검증하는 데에 어려움이 있었다. 빛으로 특정 전령RNA의 이동과 단백질 합성을 조절하는 새로운 기술을 개발하여 Cell, Nature Biotechnology 등의 학술지에 논문을 투고했지만, 논문심사 리뷰어들이 너무나 많은 보강실험들을 요구하여 Cell에는 1년 동안 논문심사를 받았고, Nature Biotechnology에는 1년 이상 논문심사 및 수정본을 제출하였지만 게재승인을 받지 못하였다. 새로운 기술이라 효용성을 검증하는 데에 많은 시간이 걸렸고, 본 연구실에서 하지 않았던 연구라 관련 실험들을 셋팅하는데 상당한 어려움이 있었다. Nature Cell Biology에도 심사기간이 1년 정도 걸려서 본 논문이 완성되고 최종 게재 되는데 총 3년의 시간이 걸렸다.
[연구 과정]
이번 연구는 허원도 교수의 아이디어 제안으로 시작되어, 세포 내 전령RNA의 이동 및 단백질 합성을 직접 억제할 수 있는 광유전학 기술을 제시하고 최적화하는 과정을 거쳤다. 이 과정에는 제 1저자인 김나연 박사(KAIST), 공동교신저자인 이상규 박사(IBS 인지 및 사회성 연구단)가 기여했다.
[향후 연구계획]
허원도 초빙연구위원 연구팀은 이번 연구로 개발한 RNA 광유전학 기술로 전령RNA를 시공간 특이적으로 조절하고, 이를 세포 수준에서 실험동물 수준에 이르기까지 연구에 광범위하게 적용하고 있다. 향후 유전자 기능 및 신호전달 체계를 이해하는데 있어, 세포 수준부터 복잡한 신경계 등 조직 수준에 이르는 통합적인 접근과 이해를 바탕으로 실제 생체 내에서 일어나는 생명현상을 심층적으로 이해해 나가는 연구를 진행할 예정이다.
그림 설명
전령RNA에 청색광을 비추면 전령RNA가 이동을 멈추고, 단백질 합성이 저해됨. 빛을 차단하면 전령RNA의 이동과 단백질 합성이 다시 시작됨. mRNA-LARIAT 광유전학 기술로 세포 내 특정 시점 및 위치에서 전령RNA 이동과 단백질 합성의 중요성을 연구할 수 있음.
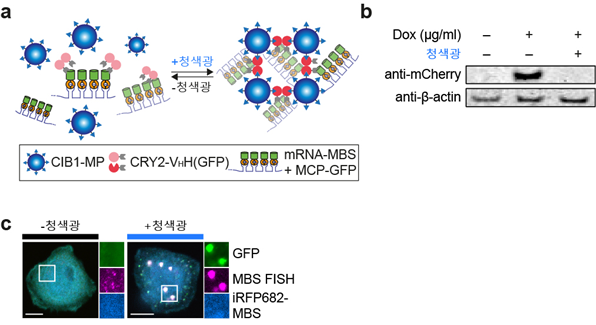
a. mRNA-LARIAT 광유전학 기술 모식도
b. mRNA-LARIAT 광유전학 기술로 단백질 합성 저해
c. 청색광에 의해 형성된 단백질-전령RNA 복합체 유도 및 전령RNA 확인
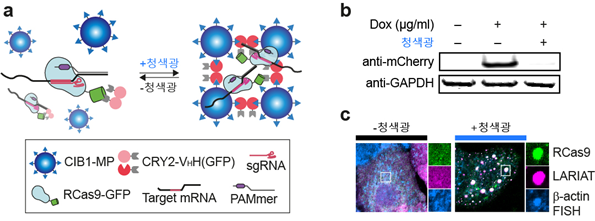
a. 내인성 전령RNA 표적을 위한 유전자 가위(RCas9) 기반의 mRNA-LARIAT 광유전학 기술 모식도
b. 유전자 가위(Cas9) 기반의 mRNA-LARIAT 광유전학 기술로 단백질 합성 저해
c. 청색광에 의해 형성된 단백질-전령RNA 복합체 유도 및 내인성 베타액틴(β-actin) 전령RNA 확인
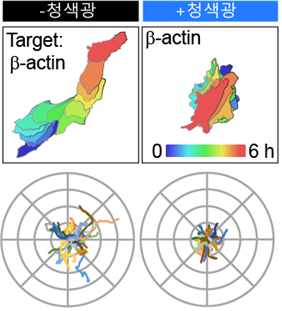
베타액틴(β-actin) 단백질 합성에 관여하는 전령RNA에 청색광을 비춰줌으로써 단백질 합성을 억제하고 세포의 이동 기능을 6시간 동안 관찰함. 베타액틴(β-actin) 전령RNA가 단백질 복합체(LARIAT)에 가둬지면 세포의 이동 기능이 현저히 감소됨. 이는 새롭게 합성된 베타액틴(β-actin) 단백질이 세포의 이동 기능에 필수적임을 의미함.
연구진 이력사항
[허원도 IBS 인지 및 사회성 연구단 초빙연구위원/ KAIST 생명과학과 교수, 교신저자]
1. 인적사항
○ 소 속 : IBS 인지 및 사회성 연구단,
KAIST 생명과학과
○ 전 화 : 042-350-2642
○ 이메일 : wondo@kaist.ac.kr
2. 학력
1987 – 1994 학사, 경상대학교 농화학과
1994 – 1996 석사, 경상대학교 생화학과
1996 – 1999 박사, 경상대학교 생화학과
3. 경력사항
1999 – 2000 Dept. of Cell Biology, Duke University, Postdoctoral Fellow
2000 – 2006 Dept. of Molecular Pharmacology, Stanford University,Postdoctoral Fellow/Research Associate/Senior Research Scientist
2006 – 2008 Dept. of Chemical and Systems Biology, Stanford University,
Senior Research Scientist
2003 – 2008 Dept. of Chemical and Systems Biology, Stanford University,Co-Investigator
2008 – 현재 KAIST 생명과학과, 조교수, 부교수, 교수
2013 – 현재 IBS 인지 및 사회성 연구단, 그룹리더, 초빙연구위원
4. 전문분야
허원도 교수는 KAIST를 부임한 이후 지난 12년 동안 “분자광유전학”이라는 독자적인 연구분야를 개척하고 있으며, 최근 5 년간, 분자광유전학분야 국내외 최상급 연구 성과를 Nature Biotechnology, Nature Methods (2편), Nature Chemical Biology, Nature Communications (6편), PNAS지 (2편)에 보고하고 있음. 세포 내 분자들을 빛으로 활성화하여 생쥐의 행동 및 기억형성/강화의 뇌과학연구를 수행하고 있음.
[이상규 IBS 인지 및 사회성 연구단 연구위원, 공동교신저자]
1. 인적사항
○ 소 속 : IBS 인지 및 사회성 연구단
○ 전 화 : 042-878-9114
○ 이메일 : sklee@ibs.re.kr
2. 학력
2001 – 2005 학사, KAIST
2005 – 2011 박사, KAIST
3. 경력사항
2011 – 2013 KAIST 생명과학과, Post-Doc
2013 – 2017 IBS 인지 및 사회성 연구단, 연구위원 (비영년직트랙)
2018 – 현재 IBS 인지 및 사회성 연구단, 연구위원 (영년직트랙)
[김나연 인지 및 사회성 연구단 연구원, 제 1저자]
1. 인적사항
○ 소 속 : 인지 및 사회성 연구단
○ 이메일 : nayeon89@kaist.ac.kr
2. 학력
2008 – 2012 학사, Pennsylvania State University at University Park
2013 – 2018 석・박사, KAIST 생명과학과
3. 경력사항
2018 – 2018 Research Fellow, IBS Center for Cognition and Sociality
2018 – Present Postdoctoral Fellow, Stanford University