나노 구조체는 다양한 분야에서 연구 및 활용되고 있다. 특별히 공중합체를 활용한 나노구조체는 약물을 함유하여 원하는 몸 속 위치에 전달하는 새로운 수단으로 주목을 받고 있다. 이러한 약물 전달 시스템에 활용하기 위해 최근 나노구조체를 설계하고 이를 효과적인 약물전달 시스템의 수단으로 삼고자 하는 연구가 활발히 진행되고 있다. 그러나 이러한 약물 전달 시스템에는 아직 여러 해결해야만 하는 과제들이 많이 남아 있다. 특별히 이러한 약물 전달 시스템의 부작용을 줄이고 그 효과를 향상시키기 위해서 약물 전달 시스템을 정밀하게 제어할 필요가 있다.
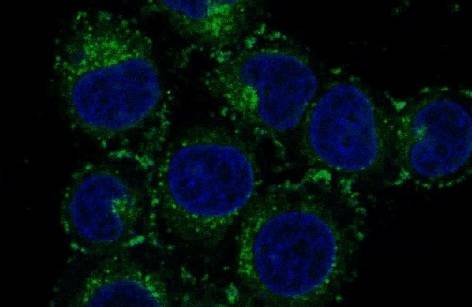
그림. 헤라 세포 내에서 산화 환원 반응의 커큐민 미셀이 흡수되는 과정을 나타내고 있다.
약물 전달 시스템에서 정확한 목표 지점에 정확하게 전달되기 전 약물의 조기 방출을 막는 것은 매우 까다로운 과제 중 하나이다. 최근 중국 연구진은 양친매성의 디설파이드를 포함하고 있는 공중합체 커큐민 접합 운반체를 통해서 이러한 약물의 전달의 정확성을 높인 새로운 연구결과를 발표했다. 연구진은 세포질 내에 높은 글루타티온 농도 아래에서 일어나는 산화 및 환원 반응을 통해서 이번 연구 성과를 얻을 수 있게 되었다. 연구진은 이러한 방법을 통해서 나노 수준에서 세포 간 전달 플랫폼을 이용하여 효과적이고 신뢰성이 높은 약물 전달 시스템을 설계할 수 있게 되었다. 이러는 기술은 미래의 임상 실험을 비롯하여 사전 약물 반응 실험에도 큰 도움이 될 수 있을 것으로 기대된다.
조기 약물 방출은 목표 지점에 도달하기 전에 합성 순환 과정에서 일어나는 활성제의 반응으로 인한 것이다. 이는 혈액이 완전한 싱크 조건을 유지하기 때문이다. 적절한 위치에 효과적으로 약물을 방출하는 것은 약물 전달 기구가 사전 약물을 방출하지 않고 목표지점까지 그 약물을 함유하고 있다가 원하는 위치와 시점에 약물을 방출하는 것을 의미한다. 이러한 것은 때때로 두 서로 다른 약물 전달 효과로 나타내어 그 효과를 서로 감쇄하는 것으로 나타나기도 한다.
이번에 중국 톈진대학(Tianjin University)과 난카이대학(Nankai University) 이스라엘 텔 아비브 대학(Tel-Aviv University) 연구진은 공동으로 이번 연구를 설계하고 진행했다. 연구진은 양친매성 폴리머 커큐민 혼성체를 자기 조립 방식으로 만들었다. 이를 통해서 세포 간 이동이 매우 빠르면서 세포 내에서 글루타티온의 활동 아래에서 분해되는 약물 전달 시스템을 만들었다. 이번 연구결과는 소수성 활성제를 만드는 데에서부터 그 밖에 다른 약물 전달 시스템에도 활용될 수 있을 것으로 기대된다.
이번 연구는 저널 Nanotechnology에 “Triggered-release polymeric conjugate micelles for on-demand intracellular drug delivery”라는 제목으로 게재되었다. (doi:10.1088/0957-4484/26/11/115101)
