13건 이상의 연구 결과 발표
투제오®, 국내 최초 고정비율 통합제제 솔리쿠아® 등 사노피 당뇨병 치료제 포트폴리오 전반 총망라
개인별 맞춤 관리를 통한 당뇨병 환자의 삶의 질 향상의 중요성 강조
㈜사노피-아벤티스 코리아(대표 배경은, 이하 ‘사노피’)는 12월 2일부터 6일까지 진행된 2019년 국제당뇨병연맹 총회(IDF Congress 2019)에서 13건 이상의 연구 데이터 발표를 통해 자사 당뇨병 치료제 포트폴리오 전반을 총망라하는 시간을 가졌다.
사노피가 이번 IDF에서 준비한 세션의 주제는 “개인별 맞춤 관리를 통한 당뇨병 환자의 건강과 삶의 질 향상의 중요성”이다. 주요 내용으로 투제오®주 솔로스타®(성분명: 인슐린글라진, 유전자재조합 300 U/mL, 이하 투제오®)의 BRIGHT 연구 사후 하위분석과 솔리쿠아®펜주(10-40)(성분명: 인슐린글라진, 유전자재조합 100U/mL 및 릭시세나티드 50 mcg/mL, 이하 솔리쿠아®)의 네트워크 메타분석 결과를 공유하는 한편, 개발도상국 성인 당뇨병 환자를 대상으로 실시된 최대 규모의 국제 관찰 연구인 IDMPS(International Diabetes Management Practices Study) 포스터 연구 4개가 발표됐다.
먼저 투제오®는 인슐린 데글루덱과의 최초 직접 비교(head-to-head) RCT(Randomized Clinical Trials)연구인 BRIGHT 연구에 참여한 환자 중 70세 이상의 제 2형 당뇨병 환자를 대상으로 조사한 사후 하위분석결과를 발표했다. 연구 결과, 투제오®군에서 -1.69%로 인슐린 데글루덱 투여군(-1.34%) 대비 평균 혈당 조절 능력이 개선되었으며, 저혈당 사건 및 발생률에 있어서도 유사한 것으로 나타났다. 이를 통해 저혈당 위험이 특히 높은 고위험의 고령 환자들에게 투제오®가 새로운 옵션으로 기능할 수 있음을 시사했다.
다음으로 국내 최초의 고정비율 통합제제(Fixed Ratio Co-formulation, 이하 FRC) 당뇨병 치료제인 솔리쿠아® 네트워크 메타분석 결과도 공유됐다. 연구에 따르면, 제2형 당뇨병 환자가 솔리쿠아®로 치료받을 경우 첫 12주 용량적정기간에 GLP-1 RA 대비 오심(nausea) 발생률이 52%에서 68%가량 통계적으로 더 낮은 것으로 나타났다.
한편, 새롭게 공개하는 내용으로 사노피는 4개의 IDMPS 연구 발표를 통해 다양한 질환적 특성을 갖는 당뇨병 환자들의 미충족(unmet) 수요 해결을 위한 자사의 노력을 강조했다. 치료제를 넘어, 개별 검사와 교육 등 당뇨병의 통합적 관리의 중요성에 대한 이 연구는 ‘제 1형 및 2형 성인 당뇨병 환자에게서 선별 검사 빈도에 따른 만성 신질환 발생정도’와 ‘제1형 당뇨병 환자의 혈당 목표치 달성에 미치는 교육 및 자기 관리의 영향’, ‘인슐린 치료를 받는 성인 제 2형 당뇨병 환자에서의 미충족 의료 요구’, ‘성인 제2형 당뇨병 환자에서 인슐린 관리를 평가하기 위한 횡단면 종단 설계(Wave 8 연구설계)’ 등을 포함하고 있다.
사노피 배경은 대표는 “사노피는 전세계 당뇨병 환자의 건강 및 삶의 질 개선을 위해, 무엇보다도 개인별 특성에 맞춤화 된 치료를 발전시킬 수 있는 방향으로 개발 및 연구의 중점을 두고 있다”며 “이번 IDF에서 발표한 다수의 연구 데이터가 이 같은 방향성에 기여할 수 있는 밑거름이 되기를 기대하며, 앞으로도 당뇨병 관리에 가장 효과적으로 기여할 수 있는 솔루션을 개발하기 위해 노력하겠다”라고 말했다.
한편 국제당뇨병연맹(IDF)은 전세계 168개국, 240개가 넘는 당뇨병협회의 국제 연맹으로, 1950년 이래로 전세계의 당뇨병 단체를 이끌며 당뇨병 관리 및 예방, 치료를 위해 활동하고 있다. 그 일환으로써 매년 총회를 개최하고 있으며 올해는 300명의 연자가 발표를 진행하는 가운데 1,000개의 포스터 세션이 진행되었다.
* 투제오® 사후 하위분석 결과 요약
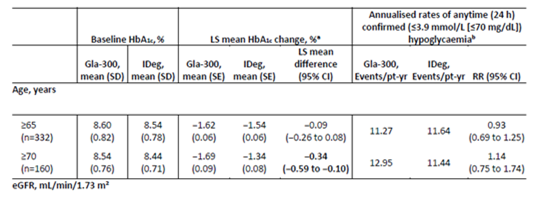
제2형 당뇨병 환자에서 인슐린데글루덱 대비 투제오®의 유효성 및 안전성을 70세 이상 환자에서 측정하여 평가했다.
- 당화혈색소(HbA1c)의 변화
- 24주기간동안 하루중(24시간) 확인된 저혈당(≤3.9 mmol/L [≤70 mg/dL]) 사건(event rate) 및 발생률
투제오®는 확인된 저혈당발생률 및 사건(event rate)에 있어 차이없이 인슐린데글루덱 대비 혈당조절(HbA1c)의 더 큰 개선을 나타내며(각각-1.69% vs. -1.34%), 통계상으로 유의한 0.34%의 추가적인 감소를 나타냈다.
24주 연구기간 동안의 당화혈색소 변화 및 저혈당 사건
이 새로운 데이터는 중등도 및 중증 신기능장애(eGFR <60 mL/min/1.73 m2)를 동반한 성인 제2형 당뇨병 환자에서 이전에 보고된 결과를 더욱 확대시키는 것이다. 투제오®는 이 환자군에서 확인된 저혈당 발생률 또는 사건의 차이 없이 인슐린데글루덱 대비 당화혈색소의 43% 감소가 관찰됐다(각각-1.72% vs.-1.30).1
BRIGHT는 투제오®(466명) 또는 인슐린데글루덱(463명)으로 무작위배정된 제2형 당뇨병 환자를 대상으로 실시된 다기관, 오픈라벨, 공개표지, 활성대조, 평행군 임상시험이었다. 별도로 보고된 결과에서 모든 일차 및 이차 평가변수가 충족되었다.5,6이 전체연구에서 참가자들은 2개 치료제를 통해 유사한 평균 혈당감소를 달성했으며, 용량적정기간(0-12주) 동안 투제오®에서 저혈당사건이 더 낮았다.6
* 솔리쿠아® 네트워크 메타분석 연구결과 요약2
베이지안 네트워크메타분석(NMA)을 사용하여 17건의 발표임상 시험에서 나온 데이터를 기반으로 치료 처음 12주(용량적정기간) 동안 오심에 대한 누적데이터를 모형화했다. 사용된 임상시험은 전반적으로 연령, 기저점 당화혈색소(HbA1c), 기타 임상적 특성에 있어 유사했다. 솔리쿠아®와의 비교는 개별 GLP-1 RA에 대해 이루어졌으며(TSN: Treatment Specific Network 모형), 단기 및 장기 지속형으로 분류되었다(DCN: (Drug Class Network 모형).
TSN(고정효과) 모형을 사용했을 때 솔리쿠아®로 치료받은 환자에게서 주 1회 투여하는 엑세나타이드 2mg을 제외한 모든 GLP-1 RA보다 오심발생률이 낮았다(엑세나타이드2mg과는 유의한 차이 없었음).
솔리쿠아® 치료시 아래의 용량적정된 약물대비 오심발생률 감소에 있어 다수의 유의미한 차이가 나타났다.
- 엑세나타이드 10μg (rate ratio [RR]: 0.32, 95% 신뢰구간: 0.15 to 0.66)
- 릭시세나티드 20μg (0.35; 0.24-0.50)
- 리라글루티드 1.8mg (0.48; 0.23-0.98)
- 세마글루타이드 1mg (0.60; 0.30-1.23, 유의하지 않음)
- 둘라글루타이드 1.5mg (0.60; 0.29-1.26, 유의하지 않음)
- 엑세나타이드 2mg (1.91; 0.91-4.03, 유의하지 않음)
DCN(무작위효과) 모형에서 GLP-1 RA 대비솔리쿠아® 치료시 오심발생률이 22-50% 낮은 것으로 나타났다. 하지만 이는 통계적으로 유의미하지 않았다. (RR = 0.50 vs 단기지속형 GLP-1 RA, 95% 신뢰구간: 0.12-3.10; RR = 0.78 vs 장기지속형 GLP-1 RA, 95% 신뢰구간: 0.17-5.29)
이전에 발표된 임상시험데이터의 네트워크메타분석으로써, 연구에서 치료에 대한 어떠한 다른 이상반응은 평가되지 않았다. 위장관계반응(오심, 구토 그리고 설사)이 GLP-1 RA의 확립된 안전성프로필 내에서 가장 흔한 이상반응이었으며, 솔리쿠아® 임상시험에서 저혈당 또한 기록된 것으로 보고됐다.
References
1. Cheng A et al. Oral posterOP-0081, International Diabetes Federation (IDF) Congress2019, December 2-6, 2019, Busan, South Korea.
2. Rayner CK, et al. Poster presentation P-0438, World Diabetes Federation Congress, Wednesday, December 4, 2019, Busan, South Korea
3. Data on file: IDF Curtain Raiser
6. Rosenstock J, et al. Diabetes Care. 2018;41(10):2147-54, DOI: 10.2337/dc18-0559
7. Haluzik M, et al. Oral presentation #146-OR, American Diabetes Association 79th Scientific Sessions, Sunday, June 9, 2019, San Francisco, CA, U.S
8. 식품의약품안전처, 의약품화장품전자민원창구정보마당, 제품상세정보, 투제오
10. Riddle M., et al. (EDITION 1). Diabetes Care. 2014;37:2755-62.
11. Yki-JärvinenH.,et al. (EDITION 2). Diabetes Care. 2014;37:3235-43.
12.
13. Bolli GB., et al. (EDITION 3). Diabetes ObesMetab. 2015;17:386-94.
14. Home PD., et al. (EDITION 4). Diabetes Care. 2015;38:2217-25.
15. Matsuhisa M., et al. (EDITION JP1) Diabetes ObesMetab. 2016;18:375-83.
16. Terauchi Y., et al. (EDITION JP2). Diabetes ObesMetab. 2016;18:366-74.
17. 1095-P: Early Hypoglycemia after Initiation of Second-Generation Basal Insulin (BI) Analogs: Patient Characteristics and Clinical Outcomes, Diabetes 2019 Jun; 68(Supplement 1):
18. Mauricio D et al. Glycemic control and hypoglycemia burden in patients with type 2 diabetes initiating basal insulin in Europe and the USA. Diabetes ObesMetab. 2017 Mar 2. doi: 10.1111/dom.12927. [Epub ahead of print]
19. 식품의약품안전처, 의약품/화장품전자민원청구, 정보마당, 의약품등정보, 제품정보, 솔리쿠아펜주(10-40), 솔리쿠아펜주(30-60)
20. SOLIQUA SmPC, March 2017
21. Vanita R. Aroda et al. Diabetes Care 2016;39(11):1972-1980