화학반응 에너지, 열로 사라지지 않고 기계적 에너지로 전환
초소형 세계의 에너지 패러다임 바꿔
기초과학연구원(IBS) 첨단연성물질 연구단 스티브 그래닉 단장(UNIST 자연과학부 특훈교수)과 후안 왕 연구위원은 일반적인 화학반응에서 발생하는 에너지가 열로 모두 방출된다는 기존 상식을 뒤집고, 화학반응 뒤에 분자가 추진력을 얻어서 확산*이 가속되는 것을 밝혔다.
* 분자가 주변 분자들과 부딪히면서 생기는 무작위 움직임.
분자는 화학반응을 할 때, 원자들 사이의 기존 결합을 끊고 새 결합을 형성하면서 다른 물질로 바뀐다. 이 때 발생하는 반응에너지는 국소적인 열 형태로 발산되어 사라지고, 분자 움직임에는 영향을 주지 않는다는 것이 기존 상식이었다.
연구진은 화학반응 시 분자들의 이동을 추적하여 반응 뒤 분자 이동성이 거시적으로 증가하는 것을 발견, 반응에너지가 기계적 에너지로 전환됨을 보였다.
과학기술정보통신부(장관 최기영)와 IBS(원장 노도영)는 이번 성과가 세계 최고 권위의 학술지 사이언스誌(Science, IF 41.845)에 7월 31일 게재되었다고 밝혔다.
연구진은 액체 용매 속 화학반응에서 증가하는 분자 움직임을 관찰하고, 이 움직임이 기존의 열 방출 이론으로 설명되지 않는 동력에 의한 것임을 증명하였다.
연구진은 먼저 용매 속에서 일어나는 화학반응을 핵자기공명*으로 관찰해, 각 반응물 분자의 움직임을 추적했다. 실험 결과 반응 뒤 분자의 확산이 빨라지며, 반응 과정에서 생기는 각 분자의 확산 속도가 서로 다름을 확인했다. 이는 분자가 열 이외에 다른 동력을 가짐을 의미한다.
* 원자의 핵스핀을 감지하는 자기공명영상.
또한 연구진은 촉매가 관여하는 반응이 일반 화학반응과 전혀 다른 분자 이동을 야기하는 것도 밝혀내었다.
서로 다른 15가지 화학반응에서 나타나는 확산 속도를 분석한 결과, 촉매반응과 촉매 없는 반응의 확산 양상이 크게 달랐다.
연구진은 추가로 촉매 농도가 불균일한 미세유체칩*을 준비하고, 칩 안에서 용매 움직임을 관찰했다. 이 때 촉매 농도가 작은 쪽으로 용매가 이동했는데, 반응물 농도 기울기에서는 이러한 이동이 일어나지 않았다. 따라서 반응 횟수 때문이 아니라 촉매 자체가 일반 화학반응과 다른 분자이동을 일으킨다는 결론을 얻었다.
* 마이크로미터 지름의 미세한 관 안에서 액체 흐름을 조종해 시료를 처리하는 칩.
이번 연구는 기존의 화학반응의 에너지 개념을 다시 쓴 연구로, 화학반응에서 생기는 에너지가 물질을 이동시키는 기계적 에너지로 바뀐다는 것을 최초로 제시했다. 이는 분자 단위에서 동력이 필요한 초소형 로봇, 약물 전달 연구에 쓰일 수 있을 것으로 기대된다.
스티브 그래닉 단장은 “이번 실험에서 확인한 반응은 플라스틱 생산과 의생명공학 등에 일반적으로 쓰이는데, 여기서 분자 움직임을 조절하는 것은 경제적으로 큰 가치가 있다”고 설명했다. 후안 왕 연구위원은 “자연에 존재하는 스스로 움직이는 물질들을 이해하고, 정교한 초소형 기계를 만드는 데 기여할 수 있다” 고 말했다.
논문 정보
□ 논문명
◦ Boosted molecular mobility during common chemical reactions
□ 저자
◦ 후안 왕(제1저자, IBS), 박명곤(제2저자, IBS/UNIST), 로유 동(공동저자, IBS), 김준영(공동저자, IBS/UNIST), 조윤경(공동저자, IBS/UNIST), 츠비 틀루스티(공동저자, IBS/UNIST), 스티브 그래닉(교신저자, IBS/UNIST)
□ 주요내용
기존에 화학반응에서 발생하는 에너지가 분자 움직임에 영향을 미치지 못한다는 상식을 뒤집고, 화학반응 뒤 반응물 분자가 더 빠르게 움직임을 밝힘. 이는 일반적인 화학반응에서 반응에너지가 기계적 에너지로 쓰임을 제시한 전혀 새로운 연구로, 미시 세계에서 동력이 필요한 초소형 로봇, 약물 전달 연구에 기여할 것으로 기대.
연구 이야기
□ 이번 연구가 어떻게 시작되었나?
2017년에 동 연구단에서 효소의 움직임이 단순한 무작위 확산이 아니고, 큰 보폭으로 이동했다가 무작위 방향 움직임을 반복하는 ‘run & tumble’ 임을 처음 발견했다. (Enzyme Catalysis Produces Anti-Chemotaxis, PNAS 2017) 이 움직임은 박테리아에서 관찰되는 이동 전략이기 때문에, 아무 추진력이 없는 단순한 단백질 분자가 이러한 움직임을 보인다는 것은 상당히 놀라운 일이었다.
효소는 굉장히 큰 생체 분자고, 이 중 극히 일부에 해당하는 작용기가 촉매 역할을 한다. 때문에, 연구진은 촉매반응이 분자 움직임에 미치는 영향을 보다 근본적으로 분석하려고 시도했다. 따라서 단백질이 아닌 일반적인 분자의 화학반응과 촉매가 들어간 화학반응에서 분자 움직임을 분석했다.
□ 분자 움직임은 어떻게 관찰했나?
자기장 하에서 핵스핀이 공명하는 핵자기공명(NMR)을 이용해 서로 다른 분자들의 움직임을 추적했다. 핵자기공명을 이용한다고 해도 표지 분자를 개별적으로 하나하나 볼 수 있는 것은 아니고, 움직임을 통계적으로만 볼 수 있다. 때문에 동일한 분자들의 전체 움직임을 관찰해 확산 계수를 얻는다.
우리가 관찰하고 논문에 실은 것은 총 4가지 종류(click, Grubbs, ring-opening metathesis polymerization, Sonogashira)로 나뉘는 15가지 서로 다른 화학반응이었다. 15가지 반응은 모두 서로 다른 확산계수 변화를 나타냈는데, 이는 화학반응에서 발생하는 반응에너지와 비례하지 않았다.
높은 온도 자체가 활발한 분자 움직임으로 정의되기는 하지만, 화학반응에서 발생하는 에너지는 열의 형태로 국소적이며 빠르게 퍼져 사라진다고 생각됐다. 하지만 이번 연구에서 관찰한 확산계수는 반응에너지만으로는 설명할 수 없었고, 무엇보다 화학반응 과정에서 생겼다 사라지는 서로 다른 분자들이 다른 확산속도를 보여 열로는 설명할 수 없었다.
□ 촉매가 있는 반응과 없는 반응의 분자 움직임은 어떻게 비교했나?
연구진은 오른쪽으로 갈수록 촉매 농도가 높은 미세유체칩 환경에서 분자 움직임을 관찰했다. 칩 내부이기 때문에 핵자기공명영상은 쓰지 못하고, 표지 역할을 하는 분자를 용매 분자에 붙여 관찰했다. (분자의 화학 구조를 바꾸면 성질이 완전히 달라지기 때문에, 관찰대상인 반응물에는 붙이지 못한다.) 관찰 결과 용매는 촉매 농도가 낮은 쪽으로 몰렸다.
반면, 반응물 농도 기울기가 있는 칩에서는 이러한 현상이 나타나지 않고, 모든 공간에 걸쳐 용매가 균일하게 분포했다. 이는 촉매가 반응횟수를 촉진하는 것과 관계 없이, 촉매 자체가 분자 움직임을 다르게 만듦을 의미한다.
이를 확인하기 위해 위에 언급한 15가지 화학반응에서, 반응에너지와 확산 증가율 사이 관계를 분석했다. 확산이 반응에너지 때문인지, 아니면 다른 요인이 있는지 판별하기 위함이다. 분석 결과 촉매가 관여하는 반응과 일반 화학반응이 전혀 다른 양상을 보였다(그림 3의 파랑, 초록, 빨강이 촉매 반응). 그때문에 촉매가 일반 화학반응과 다른 메커니즘으로 추진력을 얻을 것으로 생각된다.
□ 이번 연구, 어떻게 쓰일 수 있나?
자연은 스스로 움직이는 미세한 물질들로 가득 차 있다. 이를테면 우리 몸의 세포 속에서 물질들을 이동하는 ‘키네신’이라는 단백질은 매우 단순한 구조지만 세포 안을 걸어다닌다. 생명체에 무수히 존재하는 예시에도 불구하고 사람은 이렇게 작은 초소형 기계를 설계하는 데 어려움을 겪고 있다. 이번 연구는 화학반응의 에너지를 기계적 동력으로 이용할 수 있는 가능성을 제시해, 미래 나노로봇과 스마트 물질 등에 근본적으로 기여할 수 있다.
그림 설명
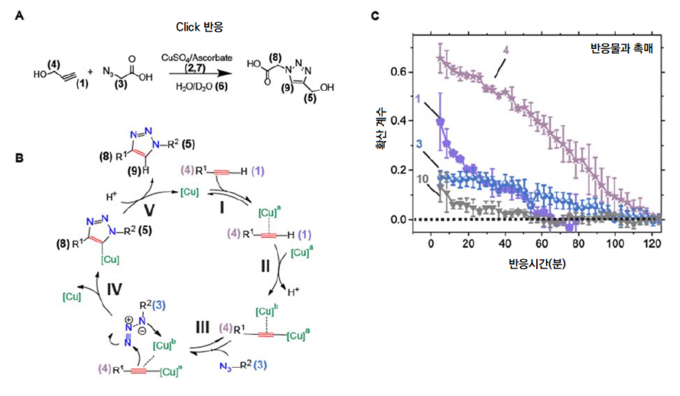
[그림 1] 화학반응 모식도와 각 분자의 확산계수
(A) 실험에서 사용된 Click 반응의 반응식. 촉매가 관여한다. (B) 자세한 반응 과정. (C) 핵자기공명영상법으로 관찰한 각 반응물과 촉매의 확산 계수 변화. 반응 시간에 따라 확산계수 감소 양상이 뚜렷하게 구별된다.
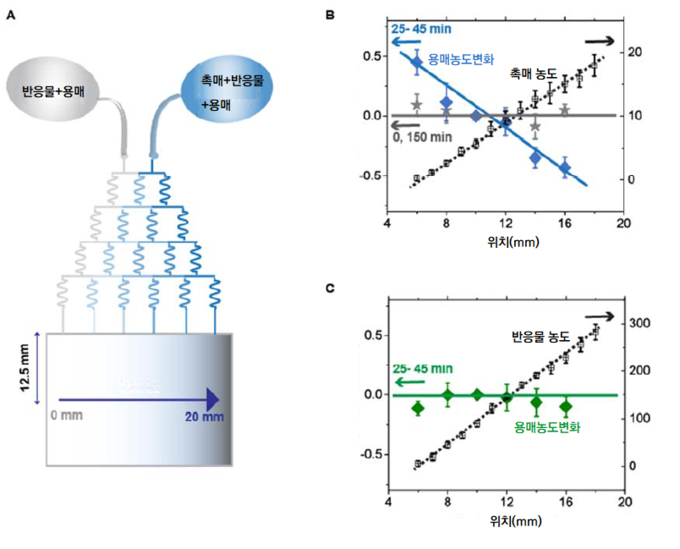
[그림 2] 촉매 농도 기울기를 가진 미세유체칩과 용매 이동
(A) 오른쪽으로 갈수록 촉매 농도가 높고, 반응물과 용매(표지) 농도는 일정한 미세유체칩 실험환경. (B) A에서 생기는 용매 농도 구배. 촉매 농도가 낮은 왼쪽으로 몰린다. (C) 대조군 실험으로 반응물 농도 구배를 주어, 오른쪽에서 반응이 더 많이 일어나는 환경을 만들었다. 그러나 촉매 구배에서 나타났던 용매 농도 구배는 없다.
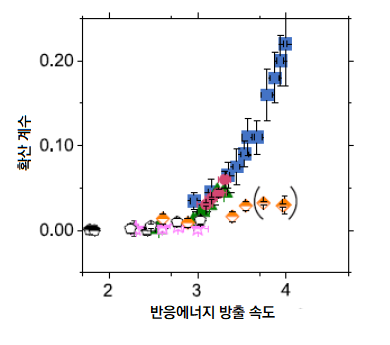
[그림 3] 6가지 화학반응의 확산 비교
서로 다른 화학반응의 반응에너지에 따른 용매의 확산계수 변화. 파랑, 빨강, 초록 점은 촉매 반응으로, 서로 일치하는 가파른 그래프를 그린다. 반면 주황, 분홍, 하양은 촉매가 없는 일반 반응으로, 완만한 그래프를 그린다.
연구자 이력사항
[스티브 그래닉 IBS 첨단연성물질 연구단장, 교신저자]
1. 인적사항
· 소속 : IBS 첨단연성물질 연구단UNIST 자연과학부
· 전화 : 052-217-5508
· e-mail : sgranick@ibs.re.kr
2. 학력
· 1978 학사, 프린스턴 대학교
· 1982 박사, 위스콘신 대학교
* 박사 재학시절 당대 최고의 고분자물리화학자 존 페리(John D. Ferry)와 공동연구
* 박사 후 과정 중 피에르-질 드젠느(1991년 노벨 물리학상 수상자)와 공동연구
3. 경력사항
· 1985 – 2014 미 일리노이 대학교 교수
· 2014 – 현재 기초과학연구원(IBS) 첨단연성물질 연구단장
· 2014 – 현재 울산과학기술원(UNIST) 자연과학부 특훈교수
4. 수상실적
· 2009 미국물리학회 고분자 물리 분야 최고상
· 2013 미국화학회 콜로이드와 표면화학 분야 최고상
· 2015 미국 국립과학원(NAS, National Academy of Science) 회원 선출
· 2016 미국 국립학술원(American Academy of Arts and Science) 회원 선출
[후안 왕 IBS 첨단연성물질 연구단 선임연구원, 제1저자]
1. 인적사항
· 소속 : IBS 첨단연성물질 연구단
· 전화 : 052-217-5518
· 이메일 : huanwang@ibs.re.kr
2. 학력
· 2009 학사, 중국 베이징 대학교
· 2015 박사, 미국 애리조나 대학교
3. 경력사항
· 2009 – 2012 애리조나 대학교, 수업 조교(T.A.)
· 2012 – 2015 애리조나 대학교, 연구 조교(R.A.)
· 2015 – 현재 IBS 첨단연성물질 연구단, 연구위원