ATTR-ACT 임상연구에서 위약군과 타파미디스메글루민염 80mg/빈다맥스로 지속 치료를 받은 환자군을 비교·평가한 사후 중간 분석 결과 미국 심장협회저널(Circulation: Heart Failure) 게재
한국화이자제약(대표이사 사장 오동욱, www.pfizer.co.kr)은 트랜스티레틴 아밀로이드 심근병증(Tranthyretin Amyloid Cardiomyopathy, 이하 ATTR-CM) 치료제 빈다맥스®(성분명: 타파미디스)와 타파미디스메글루민염이 약 5년의 장기 추적연구 중간분석 결과에서 임상적으로 유의한 장기 생존율 개선 효과를 보였다고 1월 20일 밝혔다.
빈다맥스®의 3상 연구인 ATTR-ACT 연구와 ATTR-ACT의 장기연장연구를 분석한 이번 연구결과는 지난 해 12월 미국 심장협회(American Heart Association)에서 발간하는 학술지 ‘순환: 심부전(Circulation: Heart Failure)’에 게재됐다. 1
ATTR-ACT 연구에서 타파미디스메글루민염 80mg, 타파미디스메글루민염 20mg, 위약군으로 각각 무작위 배정했으며, 연구가 완료되는 30개월 시점에서 타파미디스메글루민염 80mg 투여군은 장기 연장 연구에서 지속적으로 타파미디스메글루민염 80mg을 투여받았고, 빈다맥스 61mg 단일 캡슐 제제로 전환했다. 그리고 ATTR-ACT 연구에서 위약을 투여 받은 환자군은 타파미디스메글루민염 80mg 또는 타파미디스메글루민염 20mg 치료군에 무작위 배정(2:1) 되었다. 두 군 모두 빈다맥스 61mg 사용이 가능해진 시점에서 타파미디스메글루민염 80mg과 생물학적으로 동등한 빈다맥스 61mg 치료로 전환해 장기연장연구에 참여했다. 1
ATTR-ACT 연구에 따르면 타파미디스메글루민염은 30개월 시점에서 위약군 대비 사망 위험을 30% 감소시켰으며, 이번에 발표된 장기연장연구에서 약 5년 간(중앙값)의 장기 추적 치료 결과에 따르면 타파미디스메글루민염 80mg/빈다맥스 61mg 치료를 지속한 환자군(추적관찰 기간 중앙값 58.5개월)은 위약군에서 타파미디스메글루민염 80mg/빈다맥스 61mg로 전환한 환자군(추적관찰 기간 중앙값 57.1개월)에 비해 모든 원인에 의한 사망 위험이 41% 감소한 것으로 나타났다(HR: 0.59; 95% CI: 0.44–0.79; P<0.001). 1
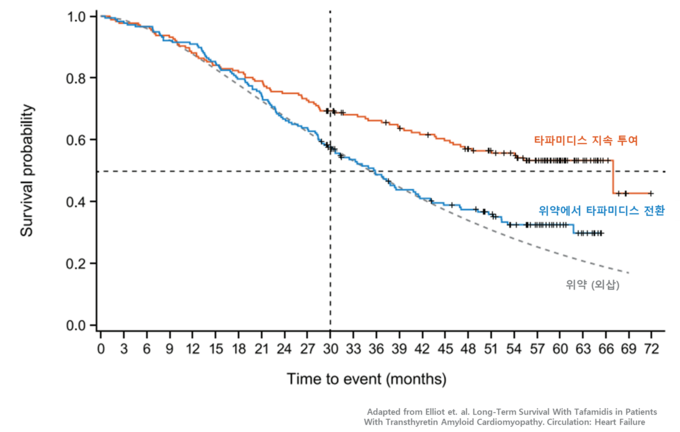
[그래프] ATTR-CM 환자의 빈다맥스 치료 장기생존 데이터1
또한, 지속 치료 환자군의 생존기간 중앙값은 67개월(95% CI: 47.0–N/E)로, 위약-치료 전환군의 35.8개월(95% CI: 29.7–41.1) 대비 30개월 이상 개선된 것으로 나타났다. 지속 치료 환자군의 5년 생존율은 53.2%로, 위약에서 빈다맥스 61mg 치료 전환군에서의 5년 생존율 32.4% 대비 의미 있는 개선을 확인했다.1
화이자 희귀질환사업부 최고개발책임자 브렌다 쿠퍼스톤(Brenda Cooperstone) 박사는 “이번 분석 결과는 중추 임상시험인 ATTR-ACT의 긍정적인 결과를 기반으로 타파미디스메글루민염 80mg과 이와 생물학적으로 동등한 빈다맥스 61mg이 ATTR-CM 환자의 생존률을 유의하게 연장시킬 수 있는 잠재력이 크다는 사실을 의미한다1,2”며, “다른 허가된 치료 옵션이 없는 ATTR-CM 환자들에게 타파미디스메글루민염 80mg/빈다맥스 61mg 치료는 질환 극복의 돌파구가 될 것이며, ATTR-ACT 연구와 이번 장기연장연구는 ATTR-CM 환자의 조기 치료가 중요함을 보여준다” 1고 말했다.
타파미디스메글루민염 80mg/빈다맥스 61mg의 유의한 사망 위험 감소 효과는 모든 하위 집단에서 일관되게 나타났다. 타파미디스메글루민염 80mg/빈다맥스 61mg 지속 치료는 정상형과 유전성 ATTR-CM 환자 각각에서 위약-치료 전환군에 비해 사망 위험을 39%(HR: 0.61; 95% CI: 0.43–0.87; P=0.006), 43%(HR: 0.57; 95% CI: 0.33–0.99; P=0.05) 낮췄다. 1
기저 시점에서 뉴욕심장협회(NYHA) 심기능 등급이 I 또는 II인 환자에서 타파미디스메글루민염 80mg/빈다맥스 61mg 지속 치료 환자군의 모든 원인에 의한 사망 위험은 위약-치료 전환군 대비 44% 감소했으며(HR: 0.56; 95% CI: 0.38–0.82; P=0.003), 기저 시점에 NYHA III 등급 환자에서는 35% 감소했다(HR: 0.65; 95% CI: 0.41–1.01; P=0.06). ATTR-ACT 연구에서 빈다켈은 위약과 유사한 안전성 프로파일을 보였으며, 장기연장연구에서도 새로운 안전성 우려가 관찰되지 않았으며, 이상사례의 발생 빈도 또한 위약과 유사했다. 1
유니버시티 칼리지 런던의 심혈관과학 연구소 연구소장 겸 심혈관 교수이자 본 분석의 주저자인 페리 엘리어트 박사는 “이번 장기연구 결과는 1차 분석에서 확인된 타파미디스메글루민염/빈다맥스의 생존 혜택 근거를 보강하고 ATTR-CM 환자의 조기 진단과 타파미디스메글루민염/빈다맥스를 사용한 조기 치료의 중요성을 강조한다며1,2”, “ATTR-CM에 대한 인식이 증가하고 진단에 대한 접근이 개선되면서 ATTR-CM의 진단 환경에는 많은 진전이 있었다. 하지만 ATTR-CM 질환 인식은 여전히 부족한 면이 있고, 이에 따라 환자들이 치료제의 혜택을 제대로 누리지 못하고 있다 “고 지적했다.
빈다맥스®는 2020년 8월 19일 식품의약품안전처로부터 정상형 또는 유전성 ATTR-CM 성인 환자의 심혈관계 사망 및 심혈관계 관련 입원의 감소에 대해 허가 받은 치료제로, 낮은 인지도로 심부전 환자에서 과소 진단되는 ATTR-CM의 치료에 승인 받은 최초이자 유일한 치료제다(2021년 12월 기준).
치명적인 진행성 희귀질환인 ATTR-CM은 불안정한 트랜스티레틴 단백질이 잘못 접혀 형성된 아밀로이드 단백질 원섬유가 심장 및 기타 신체 부위에 축적되어 발생한다. 심장에 축적된 트랜스티레틴 아밀로이드는 시간이 지남에 따라 심장 근육을 경직시켜 심부전을 초래한다.9 진단 후 치료받지 않은 환자의 기대 수명 중앙값은 약 2~3.5년이다.
* 타파미디스메글루민염 20mg 및 타파미디스메글루민염 80mg은 국내에서 정상형 또는 유전성 트랜스티레틴 아밀로이드 심근병증(ATTR-CM) 성인환자의 심혈관계 사망률 및 심혈관계 관련 입원의 감소의 목적으로 허가 받지 않았습니다.
** 빈다맥스 61mg은 타파미디스메글루민염 80mg과 생물학적으로 동등하나 밀리그램 단위로 교차 투여하는 용법은 허가 받지 않았습니다.
ATTR-ACT 연구와 장기연장연구에 대하여
제 3상 임상인 ATTR-ACT 연구는 정상형 또는 유전성 ATTR-CM을 모두 치료하기 위한 약물 치료를 연구한 글로벌, 이중맹검, 무작위 배정, 위약 대조 임상시험이다. 빈다켈 통합(80mg 및 20mg) 치료군과 위약군을 대조한 일차 분석에서, 연구의 1차 평가변수인 30개월의 기간동안 정상형 또는 유전성 ATTR-CM 환자들의 모든 원인에 의한 사망과 심혈관 관련 입원 빈도의 계층적 조합이 유의하게 감소했다. 또한 일차 분석의 개별 구성 요소에서도 빈다켈 치료가 위약군 대비 모든 원인에 의한 사망 위험과 심혈관 관련 입원 빈도를 각각 상대적으로 30%와 32% 감소시킨 것으로 나타났다. 2
ATTR-ACT 임상을 완료한 환자들은 최대 60개월 간 장기연장연구(LTE)에 등록할 수 있었다. 장기연장연구는 처음에 개방표지시험으로 ATTR-CM 환자를 대상으로 빈다켈 20mg 또는 80mg의 추가적인 안전성 데이터를 확보하고 현지에서 빈다켈이 이용 가능해질 때까지 기존ATTR-ACT 연구 등록 환자들에게 빈다켈 치료를 계속 제공하기 위해 설계되었다. 이후 장기연장연구의 임상시험계획서가 수정되어 빈다켈 20mg 또는 80mg 치료 환자들은 빈다맥스 단일 캡슐 61mg 치료로 전환되었다. 그리고 ATTR-ACT 연구에서 위약을 투여 받은 환자군은 타파미디스메글루민염 80mg 또는 타파미디스메글루민염 20mg 치료군에 무작위 배정(2:1) 되었다. 배정(2:1) 되었다. 두 군 모두 빈다맥스 61mg 사용이 가능해진 시점에서 타파미디스메글루민염 80mg과 생물학적으로 동등한 빈다맥스 61mg 치료로 전환해 장기연장연구에 참여했다.1
빈다켈® (성분명: 타파미디스 메글루민염)
빈다켈®(성분명: 타파미디스 메글루민염)은 2015년 국내 식품의약품안전처로부터 트랜스티레틴 가족성 아밀로이드성 다발신경병증(ATTR-PN) 치료제로 허가 받았고, 권장 용량은 20mg으로 1일 1회 1캡슐 복용한다.
빈다켈® 제품 정보: Vyndaqel® Capsule 빈다켈® 캡슐 20mg | 한국화이자 (pfizer.co.kr)
빈다맥스® (성분명: 타파미디스)
빈다맥스® (성분명: 타파미디스)는 경구형 트랜스티레틴 안정제로서, 트랜스티레틴에 선별적으로 결합하여 트랜스티레틴 운반 단백질의 테트라머를 안정시키고, ATTR-CM을 야기하는 아밀로이드 형성을 늦춘다. 빈다맥스®는 1일 1회 복용하는 61mg 캡슐형 경구제다.6
빈다맥스® 제품 정보: Vyndamax®Capsule 빈다맥스®캡슐 | 한국화이자 (pfizer.co.kr)
한국화이자
한국화이자제약은 글로벌 제약업계를 선도하는 화이자 주식회사(Pfizer Inc.)의 한국법인으로 내과질환, 염증 및 면역질환, 희귀질환, 백신, 항암제, 병원사업부 등 6개 사업부에서 신약 및 주요 치료제를 국내 환자들에게 공급하고 있으며, 자사의 기업 가치인 ‘환자들의 삶을 변화시키는 혁신(Breakthroughs that Change Patients’ Lives)’을 실현하기 위해 우수한 파트너들과 협력하여 다양한 파이프라인을 끊임없이 연구 및 개발하고 있다.
한국화이자제약은 최고의 제품과 차별화된 서비스, 업계를 선도하는 프로그램을 통해 고객 만족을 꾸준히 개선해 나아가고 있으며, 변화하는 환경에서 보다 효율적이고 전문화된 R&D 발전 및 혁신적인 보건 환경 조성을 위해 △과학 분야의 핵심역량 강화에 집중, △전략적인 파트너십 강화, △맞춤의학을 통한 차별화된 혁신/파이프라인을 추구하고 있다. 또한 책임 있는 기업 시민으로서 더불어 건강하고 행복한 사회를 만들어 나가고자 다양한 사회공헌활동을 통해 한국 사회가 추구하는 가치를 공유하고 윤리 경영을 실현하기 위한 지속적인 노력을 기울이고 있다. www.pfizer.co.kr
References
1 Elliot et. al. Long-Term Survival With Tafamidis in Patients With Transthyretin Amyloid Cardiomyopathy. Circulation: Heart Failure. 2021;0:CIRCHEARTFAILURE.120.008193
2 Maurer, Mathew S., et al. Tafamidis treatment for patients with transthyretin amyloid cardiomyopathy. New England Journal of Medicine 379.11 (2018): 1007-1016.
3 Bishop, Eve, et al. "Seven factors predict a delayed diagnosis of cardiac amyloidosis." Amyloid 25.3 (2018): 174-179.
4 Maurer MS, Elliott P, Comenzo R, Semigran M, Rapezzi C. Addressing Common Questions Encountered in the Diagnosis and Management of Cardiac Amyloidosis. Circulation. Apr 4 2017;135(14):1357-1377.
7 Mathew S, et al. Tafamidis Treatment for Patients with Transthyretin Amyloid Cardiomyopathy. N Engl J Med. 2018;379:1007-16
8 Brunjes, Danielle L., et al. "Transthyretin cardiac amyloidosis in older Americans." Journal of cardiac failure 22.12 (2016): 996-1003.
9 Grogan M, Scott CG, Kyle RA, et al. Natural history of wild-type transthyretin cardiac amyloidosis and risk stratification using a novel staging system. Heart Fail Rev. 2015 March; 20(2): 163–178.