한국얀센은 5월 23일 온오프라인을 통해 동시에 진행된 기자간담회를 통해 국내 첫 EGFR 엑손 20 삽입 변이 비소세포폐암 치료제 리브리반트™주(성분명: 아미반타맙, Amivantamab; 이하 리브리반트)’의 국내 출시를 알렸다.
이날 행사에서는 연세암병원 폐암센터장 조병철 교수(연세대학교 세브란스병원 종양내과)와 한국얀센 의학부 고민정 상무가 연자로 나서 각각 △EGFR 엑손 20 삽입 변이 비소세포폐암의 최신 지견과 리브리반트 개발을 위한 국내 연구진의 노력, △EGFR 엑손 20 삽입 변이 비소세포폐암의 새로운 치료옵션으로서 리브리반트의 허가사항 및 임상연구 결과를 주제로 발표했다.
리브리반트 적응증 및 작용 기전
리브리반트는 EGFR 엑손 20 삽입 변이 비소세포폐암 치료에 최초로 승인된 완전 인간유래 이중특이적 항체다., 지난 2022년 2월 식품의약품안전처로부터 백금 기반 화학요법 치료 중 또는 치료 이후 질병이 진행된 표피성장인자수용체(Epidermal Growth Factor Receptor, 이하 EGFR) 엑손 20 삽입 변이가 있는 국소 진행성 또는 전이성 비소세포폐암 환자의 치료에 사용하도록 허가 받았다.1
리브리반트는 EGFR 과 MET을 직접 표적하는 작용 기전으로 리간드 결합을 차단하고 EGFR, MET의 분해를 향상시켜 신호전달 기능을 방해한다.1,2, 이를 통해 종양 성장을 효과적으로 억제하고 종양 세포의 사멸을 유도한다.1,2
EGFR 엑손 20 삽입 변이 비소세포폐암
EGFR 엑손 20 삽입 변이 비소세포폐암은 기존에 승인된 치료제가 없었고, 기존 EGFR 타이로신 키나아제 억제제(Tyrosine Kinase Inhibitor, TKI)는 대부분 효과적이지 않았다. 이러한 이유로 EGFR 엑손 20 삽입 변이 비소세포폐암 치료에는 높은 미충족 의료 요구가 존재해 왔다.
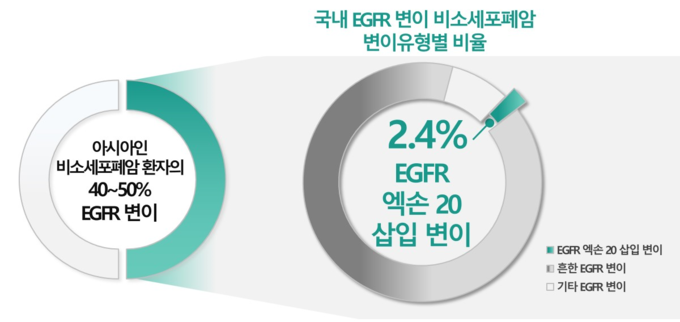
EGFR 유전자 변이는 비소세포폐암에서 가장 흔하게 발생하는 변이 중 하나며, 전세계 비소세포폐암 환자의 약 33%가 EGFR 변이를 보인다. 백인 비소세포폐암 환자의 약 10-20%에서 EGFR 유전자 변이가 관찰되는 반면, 우리나라를 비롯한 아시아인 비소세포폐암 환자에서는 이보다 더 많은 약 40~50%에서 EGFR 유전자 변이를 보이는 것으로 알려져 있다.10, 국내에서는 EGFR 변이 비소세포폐암 환자의 약 2%만이 엑손 20 삽입 변이로 진단될 정도로 드물게 나타난다.10,
EGFR 엑손 20 삽입 변이 비소세포폐암은 엑손 19 결손 및 L858R 치환 변이와 같은 흔한 EGFR 변이 폐암에 비해 예후가 좋지 못한 것으로 알려져 있다.4,5,6,7,8 EGFR 엑손 20 삽입 변이 진행성 비소세포폐암 환자의 리얼월드 전체생존기간(real world Overall Survival, rwOS) 중앙값은 16.2개월(95% CI: 11.0 – 19.4)로, EGFR 엑손 19 결손 및 L858R 치환 변이와 같은 흔한 EGFR 변이 비소세포폐암 환자의 25.5개월(95% CI: 24.5 – 27.0)보다 짧다.
1상 임상시험 ‘CHRYSALIS’
리브리반트의 EGFR 엑손 20 삽입 비소세포폐암 치료에 대한 허가는 다기관, 라벨 공개, 복수 코호트 1상 임상시험 CHRYSALIS 연구의 단독요법군에서 나온 데이터를 기반으로 한다. 기존의 표준적인 검사법으로 EGFR 엑손 20 삽입 변이를 가진 것으로 진단되었으며, 백금기반 화학요법 진행 중 또는 이후에 질병이 진행한 국소진행성 또는 전이성 비소세포폐암 환자 81명을 대상으로 유효성을 평가하였다.1,2 임상시험의 주요 목표는 눈가림된 독립적 중앙 검토위원회(Blinded Independent Central Review, BICR)가 평가한 고형암 반응평가 기준(RECIST v1.1)에 따른 전체반응률(Overall Response Rate, ORR) 평가였다.1,2 추적기간 중앙값은 9.7개월이다.1,2
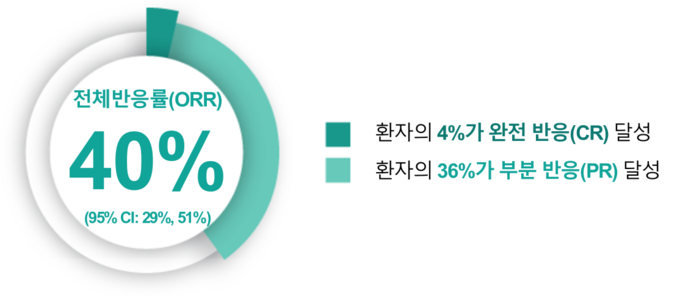
CHRYSALIS 연구 결과, 리브리반트 단독요법군의 전체반응률(ORR)은 40%(95% CI: 29 – 51)였다. 참여 환자의 4%가 완전 반응(Complete Response, CR)을 보였으며, 36%가 부분 반응(Partial Responses, PR)을 달성했다.1,2
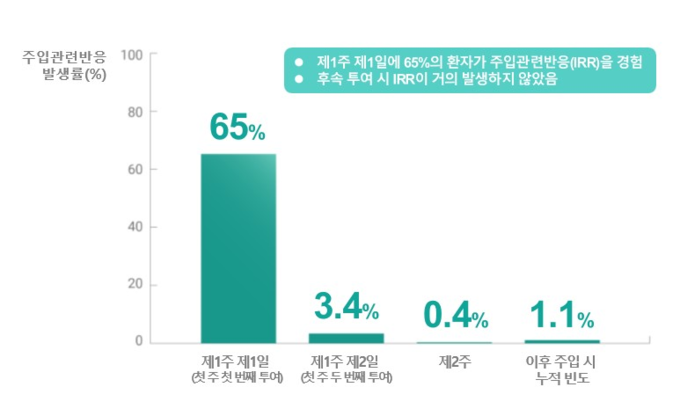
리브리반트는 임상연구를 통해 EGFR 엑손 20 삽입 변이 환자에서 지속적인 반응 및 관리 가능한 수준의 안전성 프로파일을 나타냈다.2 임상연구에서 가장 흔하게 보고된 이상반응(≥20%)은 발진(84%), 주입관련반응(64%), 손발톱주위염(50%), 근골격 통증(47%), 호흡곤란(37%), 오심(36%) 등이었다.1
존슨앤드존슨 제약부문 법인 얀센(Janssen Pharmaceutical Companies)에 대하여
얀센은 ‘질병이 과거의 일이 되는 미래’를 만들어가고 있다. 얀센은 과학과 함께 질병과 싸우고, 독창적으로 접근성을 향상시키며, 절망을 치유하는 따뜻한 마음으로 전 세계 환자들에게 건강한 미래를 선사하기 위해 끊임없이 노력하고 있다. 가장 큰 변화를 기대할 수 있는 치료 분야로 심혈관·대사, 면역, 감염병·백신, 신경과학, 종양학, 폐동맥고혈압 등에 집중하고 있으며, 자세한 내용은 한국얀센 홈페이지 (www.janssen.com/korea)를 통해 확인할 수 있다. 한국얀센은 존슨앤드존슨의 제약부문 법인 중 하나다.
* EGFR: 표피성장인자수용체(Epidermal Growth Factor Receptor)
References
1 RYBREVANT® Prescribing Information. Janssen Korea Ltd.(2022).
2 Keunchil Park et al. Amivantamab in EGFR Exon 20 Insertion–Mutated Non–Small-Cell Lung Cancer Progressing on Platinum Chemotherapy: Initial Results From the CHRYSALIS Phase I Study. Journal of Clinical Oncology. (2021).
3 Moores SL, Chiu ML, Bushey BS, et al. A novel bispecific antibody targeting EGFR and cMet is effective against EGFR inhibitor–resistant lung tumors. Cancer Res. 2016;76(13):3942-3953.
4 Remon, J et al. EGFR exon 20 insertions in advanced non-small cell lung cancer: A new history begins. Cancer Treatment Reviews. 90 (2020).
5 Baraibar I et al. Novel drugs targeting EGFR and HER2 exon 20 mutations in metastatic NSCLC. Critical Reviews in Oncology. (2020).
6 O’Leary C, Epidermal Growth Factor Receptor (EGFR)-Mutated Non-Small-Cell Lung Cancer (NSCLC). Pharmaceuticals. 2020, 13, 273; doi:10.3390/ph13100273 (2020).
7 Oxnard, JR et al. Natural history and molecular characteristics of lung cancers harboring EGFR exon 20 insertions. J Thorac Oncol. 2013 Feb;8(2):179-84. doi: 10.1097/JTO.0b013e3182779d18. (2013).
8 Simon Vyse, et al. Targeting EGFR exon 20 insertion mutations in non-small cell lung cancer. Sig Transduct Target Ther 4, 5 (2019).
9 Pennell NA, Arcila ME, Gandara DR, West H. Biomarker testing for patients with advanced non-small cell lung cancer: Real-world issues and tough choices. Am Soc Clin Oncol Educ Book. 2019;39(39):531-542.
10 Seonggyu Byeon et al. Clinical Outcomes of EGFR Exon 20 Insertion Mutations in Advanced Non-small Cell Lung Cancer in Korea. Cancer Res Treat 2019 Apr; 51(2):623-631
11 Gustavo Werutsky et al. P1.08: Updated Analysis of Global Epidemiology of EGFR Mutation in Advanced Non-Small Cell Lung Cancer. Journal of Thoracic Oncology Vol. 11 No. 10S. S184-S185, OCTOBER 01, 2016
12 Zhen Chen et al. Comparison of clinicopathologic characteristics between patients with EGFR exon 19 deletion and EGFR L858R mutation in lung cancer. Int J Clin Exp Pathol 2018;11:4644-4649
13 Fang W et al. EGFR exon 20 insertion mutations and response to osimertinib in non-small-cell lung cancer. BMC Cancer 2019;19:595.
14 S Yoon et al. Clinical Characteristics, Treatment Patterns and Outcomes of EGFR exon 20 insertion and other EGFR mutations in Korean a NSCLC Patients Abstract Book of the European Lung Cancer Congress (ELCC) volume 33 supplement 2 p50. (2022.04)
15 Bazhenova L, Minchom A, Viteri S, et al. Comparative clinical outcomes for patients with advanced NSCLC harboring EGFR exon 20 insertion mutations and common EGFR mutations. Lung Cancer. 2021;162:154-161. (2021).