“HIV 2제요법 시대 본격 개막”
HIV 치료제 개발로 기대수명 증가,
장기적 다중약물요법 영향을 최소화하는 것이 최신 개발의 경향
글로벌 3상 연구 GEMINI1, 2, TANGO를 비롯,
5,000명 이상 감염인 대상으로 하는 다중 RWD 통해
3제요법과 동등한 2제요법의 효과와 안전성 입증
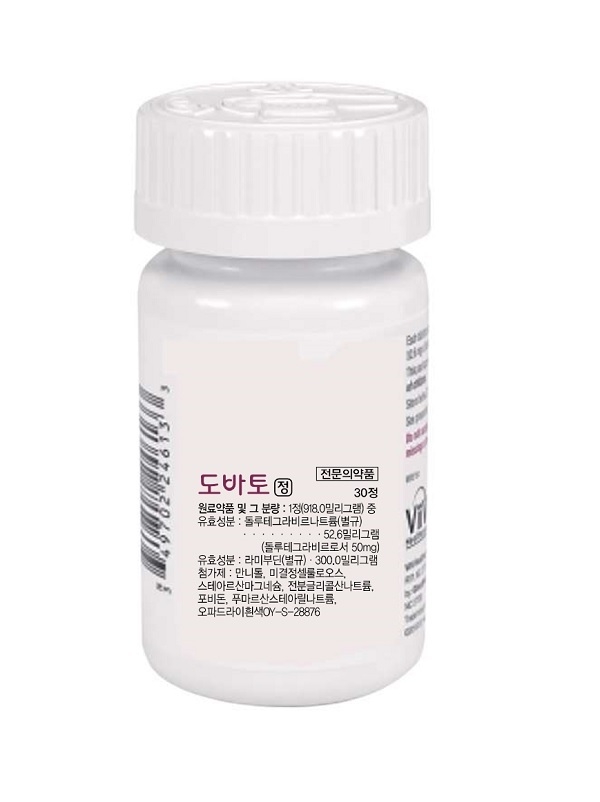
6월 23일, GSK가 차세대 HIV 치료제 ‘도바토(Dovato, 돌루테그라비르 50mg, 라미부딘 300mg)’의 론칭 기자간담회를 개최하고, 국내 첫 2제요법 단일정 치료제의 본격 도입을 알렸다.
GSK의 HIV 전문기업 비브 헬스케어(ViiV Healthcare)가 개발한 도바토는 지난 3월 국내 허가되었다. 이는 6월부로 건강보험 급여 목록에 등재되어 약가는 1 타블렛 기준 1만 8,528원으로 정해졌다.
1일 1회 1정 복용하는 도바토는 돌루테그라비르(dolutegravir, DTG)와 라미부딘(lamivudine, 3TC) 등 두 성분의 단일정으로, 신규 감염인 및 기존 치료제 경험 감염인을 위한 첫 2제요법 단일정이다.
이날 기자간담회는 코로나19 확산 방지를 위한 ‘생활 속 거리두기’ 준칙을 준수하였으며, 동시에 업계 최초로 홀로그램 영상 송출 방식을 도입해 영국 런던 내 연자의 강연과 질의응답 세션을 생중계했다.
연자로 나선 비브 헬스케어의 잔 반 바이크(Jean Van Wyk)는 돌루테그라비르 부문을 담당하는 글로벌 메디컬 디렉터로 HIV/AIDS 치료의 최신 지견과 함께 도바토의 개발 배경이 된 주요 임상 결과를 설명했다.
잔 반 바이크는 “HIV 치료제가 빠르게 발전하면서 감염인들의 기대수명이 증가하고 있다. 특히 최근 한국 내 데이터에서도 알 수 있듯 감염인 연령대가 20~30대로 젊어지고 있어 장기적인 다중약물요법(polypharmacy)의 영향을 최소화하는 것이 최근 HIV 치료제 개발의 주된 경향”이라며, “장기적 치료패턴이 주요해짐에 따라 도바토는 ARV(항바이러스제)의 장기 복용에 부담을 느끼는 감염인들의 미충족 수요에 주목했다”고 말했다.
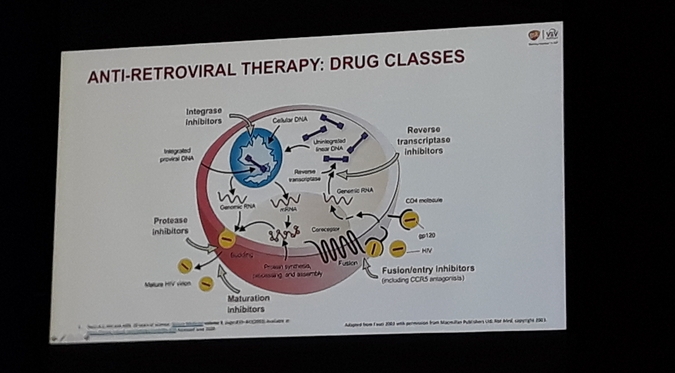
아울러 도바토의 개발과 관련해 “GSK와 비브 헬스케어는 임상에서 ARV 약물의 개수를 줄이거나 혹은 용량을 줄이거나, PK 부스터 사용을 중단하는 등 수많은 전략을 검토하였다”며, “이 중 인터그라제 억제제(INSTI)인 돌루테그라비르와 뉴클레오시드역전사효소 억제제(NRTI)인 라미부딘(3TC)이 약동력학(PK)적 프로필이 유사한 동시에 서로 다른 작용기전으로 상호 보완적 치료효과를 보인 최적의 조합이었다. 이렇게 탄생한 도바토는 랜드마크 연구인 GEMINI1,2, TANGO를 비롯해 총 5,000명 이상의 감염인을 대상으로 한 다수의 RWD(Real World Data)를 통해서 임상현장의 실제적 안전성과 효과를 함께 검증했다”고 말했다.
도바토는 신규 성인 HIV 감염인 1,400여명을 대상으로 진행된 글로벌 3상 임상시험인 GEMINI 1, GEMINI 2를 통해 기존 3제요법 (돌루테그라비르, 테노포비르 디소프록실 푸마르산염, 엠트리시타빈) 투여군 대비 동등한 항바이러스 효과 및 안전성 프로파일을 확인했다. 특히 모든 치료군에서 바이러스학적 실패를 보인 환자 가운데 치료로 인한 내성이 나타난 경우도 한 건도 없었다.
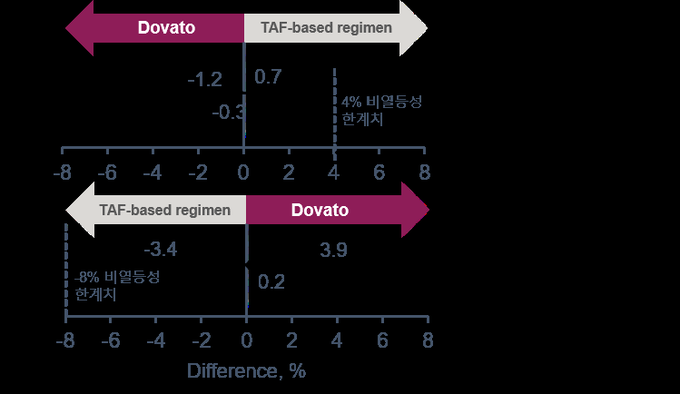
또한 도바토는 글로벌 3상 임상인 TANGO 연구를 통해 테노포비르 알라페나미드 푸마르산염(TAF)을 포함한 3제요법과 동등한 효과를 입증해냈다. TANGO 연구는 TAF를 포함한 3제요법으로 6개월 이상 바이러스 억제를 유지한 성인 감염인이 2제요법으로의 전환치료시 바이러스 억제율을 평가했다. 48주차 HIV-1 RNA 수치 50c/mL 이상인 감염인 비율에 있어 비열등성에 대한 1차 유효성 평가변수를 만족시켰으며 2제요법의 안전성 프로파일은 제품 라벨 정보와 일치했다.
이와 같은 다수의 임상 결과를 근거로 최근 미국 보건복지부(DHHS), 유럽에이즈임상학회(EACS) 등 주요 HIV 치료 가이드라인 또한 2제요법인 도바토를 1차 치료제로 권고하는 것으로 개정됐다.
줄리엔 샘슨 한국 GSK 대표는 “1987년 세계 첫 HIV 치료제인 GSK의 지도부딘이 출시되고 2제요법 단일정인 도바토가 개발되기까지 수많은 연구진들의 노력이 있었다”며, “이들 연구진과 더불어 오늘 코로나19의 상황 속에서도 취재를 위해 간담회에 참석해 주신 모든 분들에게 감사의 인사를 전한다”고 말했다.
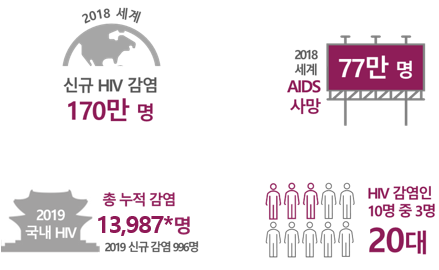
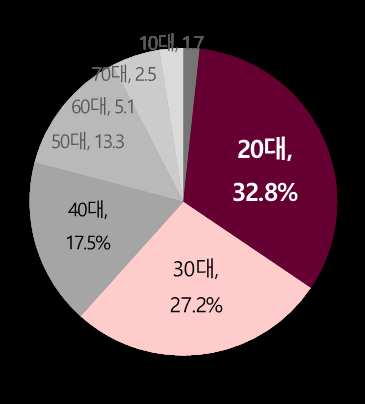
한편 질병관리본부의 자료에 따르면, 국내 누적감염자는 총 12,112명이며, 그 중 2019년 신규 감염이 996명인 것으로 나타났다. 신규 HIV 감염인의 연령대는 20대가 32.8%로 가장 많았으며, 이외에 30대(27.2%), 40대(17.5%) 순으로 조사됐다.
도바토(Dovato)에 대하여
도바토(성분명: Dovato, 돌루테그라비르50mg, 라미부딘300mg)는 이약의 개별 항레트로바이러스 성분에 대하여 알려진 또는 의심되는 내성관련 치환이 없는 성인 및 12세 이상(체중 40 kg 이상) 청소년의 인체면역결핍바이러스(HIV-1) 감염치료를 위해 허가된 첫 2제요법 복합제다. 1일 1회 1정 복용하는 도바토는 돌루테그라비르(dolutegravir, DTG)와 라미부딘(lamivudine, 3TC) 등 두성분의 단일정이다.
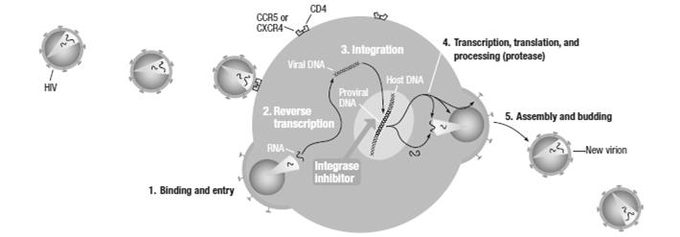
도바토는 대표적 인터그라제억제제(INSTI)인 돌루테그라비르와 뉴클레오시드역전사효소억제제(NRTI)인 라미부딘의 완전한 2제 복합제로서, HIV 복제에 필수적인 바이러스성 DNA가 인간면역세포(T세포)의 유전물질로 통합되는 것을 방해하는 동시에 바이러스성 RNA의 DNA변환을 차단해 바이러스증식을 효과적으로 저해한다.
GSK에대하여
GSK는 세계적인 연구개발 중심의 제약 및 헬스케어 회사로서, 인류가 건강장수와 행복을 추구하며 왕성하게 활동할 수 있도록 인간의 삶의 질을 향상시키는 일에 헌신하고 있다. 회사에 관한 자세한 정보는 kr.gsk.com 에서 확인할 수 있다.
비브헬스케어(ViiV Healthcare)에 대하여
비브헬스케어는 2009년 11월 글락소스미스클라인(GSK)과 화이자(Pfizer)가 HIV 감염인 및 감염관련 인류보건문제 해결을 위해 설립한 세계에서 유일한 글로벌 HIV 전문기업이다. 일본 제약기업인 시오노기(Shionogi)는 2012년 10월 주주로 참여했다. 비브헬스케어는 ‘우리는 어떠한 환자도 포기하지 않는다(Leave No PLHIV Behind)’는 비전하에, HIV 예방 및 치료, 혁신적인 치료제 공급을 위해 최선을 다하고 있다.
GEMINI 1, 2 임상에 대하여
GEMINI 1,2 임상은 1,400명 이상 HIV-1 성인 감염인이 참여한 글로벌 랜드마크 연구다. 본 임상에서 DTG + 3TC 복합요법은 치료경험이 없는 HIV-1 성인감염인 대상 HIV-1 바이러스억제 정도를 측정하는 기준인 혈장HIV-1 RNA 수치 50c/mL 미만 기준 DTG + 뉴클레오시드역전사효소억제제(NRTI) 2제 (테노포비르디소프록실푸마르산염/엠트리시타빈 [TDF/FTC]) 병용요법대비 96주차에 비열등함을 보였다. GEMINI 1과 2에서 나타난 DTG + 3TC 요법의 안전성프로파일은 DTG, 3TC 제품라벨 정보와 일치했다. 모든 치료군에서 바이러스학적 실패를 경험한 감염인 가운데 치료관련 내성은 나타나지 않았다.
TANGO 임상에대하여
TANGO 3상임상은 TAF 포함 3제요법에서 바이러스가 억제된 성인 HIV 감염인이 돌루테그라비르/라미부딘 2제요법 전환시의 항바이러스 효과와 안전성을 평가하기 위한 무작위, 오픈라벨, 능동제어, 다기관연구다. 참여자들은 148주간 무작위로 돌루테그라비르/라미부딘 요법으로 전환하거나, TAF 포함 요법을 유지하도록했다. TANGO 임상에서 돌루테그라비르와 라미부딘 2제요법은 테노포비르알라페나미드푸마르산염(TAF)을 포함한 3제요법과 동등한 효과를 나타냈다. TANGO는TAF포함 3제요법으로 6개월 이상 바이러스억제를 유지한 HIV 성인감염인이 2제요법으로 스위칭했을 때 바이러스억제율을 평가했다. 48주차 HIV-1 RNA 수치 50c/mL 이상인 감염인 비율에 있어서는 비열등성에 대한 1차유효성 평가변수를 만족시켰으며, 2제요법의 안전성 프로파일은 제품라벨 정보와 일치했다
Important Safety Information for Dovato
돌루테그라비르 관련 과민반응 : 돌루테그라비르 투여 시 과민반응이 보고되었는데, 발진과 전신 소견, 때때로 중증의 간 반응을 포함한 장기 기능이상을 특징으로 하였다. 과민반응의 징후 또는 증상이 발생하면 (중증의 발진이나 간 효소의 상승을 수반한 발진, 발열, 전신권태감, 피로, 근육통, 관절통, 수포, 구강병변, 결막염, 안면부종, 호산구증가증, 혈관부종을 포함하나 이에 국한되지는 않음), 이 약과 다른 의심되는 약물의 투여를 즉시 중단해야 한다. 간 아미노전이효소 및 빌리루빈을 포함한 임상 상태를 모니터링해야 한다. 과민반응 발현 후 이 약 또는 다른 의심되는 약물의 투 여 중단이 지연되면 생명을 위협하는 알레르기반응이 유발될 수도 있다. 다음 환자에는 투여하지 말 것 1) 이 약 또는 이 약의 성분에 과민증이 있는 환자, 2) 도페틸라이드와 병용투여해서는 안 된다.
라미부딘 관련 경고 : 1) 뉴클레오시드 유사체를 단독투여 하거나 이 약이나 다른 항레트로바이러스제와 병용하는 경우에 치명적인 사례를 포함하여 유산산증과 지방증을 동반하는 중증 간비대가 보고되있다. 2) HIV와 B형간염 바이러스가 동시 감염된 환자에게서 이 약의 투여 중단 후 B형간염의 중증 급성 악화가 보고되었다. 3) 췌장염을 암시하는 증상(심한 복부통증, 구역/구토)이나 실험실적 수치 이상(혈청아밀라제, 혈청리파아제, 중성지방 상승 등)이 나타나면 이 약의 투여를 즉시 중단해야 한다. 4) 항레트로바이러스제로 병용치료를 받는 환자에서 중심비만증, Buffalo hump, 말초소모증, 얼굴소모증, 유방 확장, 혈청 지질 및 혈당 상승을 포함한 체지방 재분배/축척이 개별적으로 또는 동시에 관찰되었다 2. 다음 환자에는 투여하지 말 것: 이 약 및 이 약의 구성성분에 과민반응의 병력이 있는 환자. 3. 다음 환자에는 신중히 투여할 것 1) 중등도~중증 신장애 환자 2) HIV 및 B형간염 바이러스에 동시 감염된 환자 3) 만성 C형간염으로 인터페론과 리바비린 치료를 받고 있는 환자 4) 췌장염의 병력이 있는 소아 환자, 췌장염의 원인이 될 수 있는 약물을 동시에 투여 받고 있는 환자 5) 간비대, 간염 또는 비만여성과 같은 간질환의 위험인자가 있는 환자 4. 과민반응: 아나필락시, 두드러기가 나타날 수 있다. 5. 일반적 주의: 1)이 약은 단독요법으로 투여하지 않는다. 2)중등도 및 중증 신장애 환자에서 라미부딘의 용량을 조절해야 한다.
References
1 ART Collaboration. Lancet HIV 2017;4:e349-56
2 Cahn P et al, J Acquir Immune Defic Syndr 2020;83:310–318.
5 Baldin G, et al. Int J Antimicrob Agents 2019;54:728–34
6 Galizzi N, et al. Int J Antimicrob Agents 2020; In press
7 Ciccullo A, et al. Antivir Ther 2019;24:63–7
8 Baldin G, et al. J Antimicrob Chemother 2019 doi:10.1093/jac/dkz009
9 Borghetti A, et al. HIV Med 2018; doi: 10.1111/hiv.12611 [Epub ahead of print]
10 Borghetti A, et al. BMC Infect Dis 2019;19:59
13 질병관리본부, 2018년 HIV/AIDS 신고현황, 주간건강과질병제12권제33호
14 Moore et al. AIDS. 1999;13:2239–50.
15 Yuen et al. Antimicrob Agents Chemother. 2004;48:176–82.
16 Min et al. AIDS. 2011;25:1737–45.
17 EPIVIR Summary of Product Characteristics. 2018.
18 Tivicay Summary of Product characteristics. 2018.
21 질병관리본부, HIV/AIDS 치료제개발현황, 주간건강과질병제11권제33호
RWD, Real World Data; ARV, Antiretroviral; PK, Pharmacokinetics; INSTI, Integrase Strand Transfer Inhibitor; NRTI, Nucleoside Reverse-Transcriptase Inhibitors;