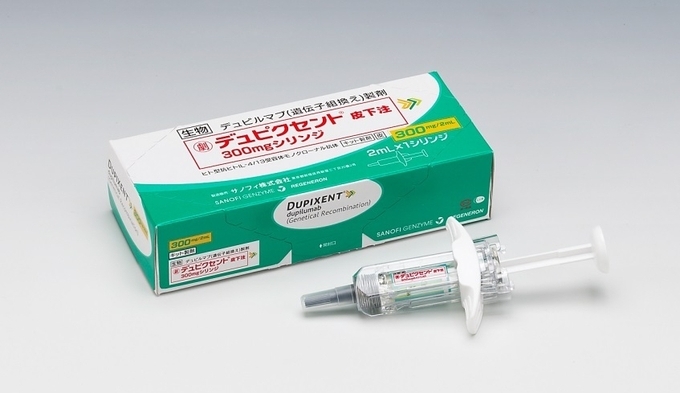
중등도-중증 성인 아토피피부염 치료제
사노피는 일본에서 지난 4월 23일 적절히 조절되지 않는 중등도-중증 성인 아토피피부염 환자를 위한 듀피젠트®프리필드주300밀리그램(Dupixent®, 성분명: 두필루맙, 유전자재조합, 이하 ‘듀피젠트®’)를 보험 급여 출시했다고 발표했다.
아토피피부염은 피부에 발진 증상을 일으키는 만성 염증성 질환이다. 특히 중등도- 중증 아토피피부염은 피부 대부분을 발진으로 덮으며, 심한 가려움증과 피부 건조, 균열, 발적, 부스럼, 진물 등을 지속적으로 동반하는 것이 특징이다. 가려움증은 환자들이 가장 고통스러워 하는 증상 중 하나로, 심할 경우 정신적 고통까지 유발할 수 있다. 이로 인해 중등도-중증 아토피피부염 환자들은 수면 장애, 불안, 우울증까지 겪고 있으며, 삶의 질이 크게 떨어지는 것으로 나타났다.
듀피젠트®는 아토피피부염의 지속적인 기저 염증을 유발하는 두 가지 주요 사이토카인(cytokine)인 인터루킨-4(IL-4)와 인터루킨-13(IL-13)의 신호 전달을 선택적으로 억제하도록 설계된 인간 단일클론 항체다. 사노피와 리제네론이 공동 개발한 듀피젠트®는 사노피의 스페셜티케어 사업부문인 사노피 젠자임(Sanofi Genzyme)이 판매할 예정이다. 듀피젠트®는 일본, 미국, 유럽연합, 캐나다, 호주와 한국에서 아토피피부염 치료제로 승인받았다.
[듀피젠트® 프리필드주 300밀리그램 일본출시 정보]
|
상표명
|
듀피젠트®프리필드주300밀리그램
|
|
성분명
|
두필루맙 (유전자재조합)
|
|
적응증
|
적절히 조절되지 않는 아토피피부염의 치료
|
|
투여량 및 투여방식
|
이약은 피하주사로 투여한다. 이약의 권장용량은 성인에서 첫회 600mg(300mg을 다른 투여부위로 연속 2회) 투여하고, 이후 2주 간격으로 300mg을 투여하는 것이다.
|
|
일본 허가일
|
2018년 1월 19일
|
|
일본 국민건강보험 급여등록일
|
2018년 4월 18일
|
|
일본 출시일
|
2018년 4월 23일
|
일본에서 사노피 젠자임을 총괄하는 파스칼 리고디(Pascal Rigaudy)는 “아토피피부염은 환자의 삶에 상당한 영향을 끼칠 정도로 몸과 마음을 약하게 만드는 질환으로, 일본의 아토피피부염 환자들을 위한 새로운 치료 옵션으로서 듀피젠트®를 출시하게 되어 매우 기쁘다”며, “사노피 젠자임은 가능한 한 빠른 시일 내에 치료가 필요한 환자들에게 듀피젠트®를 제공하기 위해 의료계와 긴밀히 협력할 것이며, 앞으로도 환자를 위한 혁신에 집중함으로써 아직 충족되지 않은 니즈를 해결하고 환자들의 삶의 질을 개선하기 위해 노력할 것”이라고 밝혔다.
한편, 듀피젠트®는 국소치료제로 적절히 조절되지 않거나 이들 치료제가 권장되지 않는 중등도에서 중증의 아토피피부염 성인 환자를 위한 치료제로 지난 3월 30일 식품의약품안전처로부터 국내 시판 허가를 받았다.